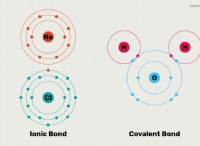
이유는 다음과 같습니다.
* 전자 구성 : 세슘은 가장 바깥 쪽 쉘에 전자가 하나뿐입니다. 이 전자는 매우 느슨하게 고정되어 있고 쉽게 손실되어 반응성이 높습니다.
* 전기 양성 : 세슘은 전기성이 매우 높으며, 이는 양의 이온을 형성하기 위해 가장 바깥 쪽 전자를 쉽게 잃게한다는 것을 의미합니다.
* 낮은 이온화 에너지 : 세슘은 이온화 에너지가 매우 낮으므로 가장 바깥 쪽 전자를 제거하는 데 최소한의 에너지가 필요합니다.
세슘과의 반응 :
세슘은 다음과 함께 격렬하게 반응합니다.
* 물 : 물과 접촉하면 수소 가스와 열을 방출합니다.
* 공기 : 그것은 공기 중에 자발적으로 산소와 질소에 반응합니다.
* 할로겐 : 그것은 염소 및 브롬과 같은 할로겐과 폭발적으로 반응합니다.
안전 예방 조치 :
세슘은 매우 위험하며 매우주의해서 다루어야합니다. 통제 된 환경에서 훈련 된 전문가 만 처리해야합니다.