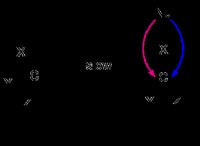
1. 용액에는 금속을 산화시킬 수있는 물질이 포함되어 있습니다. 이는 용액이 산화제를 함유한다는 것을 의미하며, 이는 화학 반응에서 전자를 얻는 물질입니다. 금속은 차례로 전자를 잃고 산화됩니다.
2. 금속은 용액의 요소보다 더 반응성입니다. 이것은 전기 화학 시리즈를 기반으로합니다. 이 시리즈의 금속이 더 높은 금속은 더 반응성이 높으며 해당 솔루션에서 시리즈의 금속을 더 낮게 대체 할 수 있습니다. 예를 들어, 황산 구리 (CUSO4) 용액에 철 (Fe)을 배치하면 철분이 전기 화학 시리즈에서 더 높기 때문에 철은 구리를 대체합니다.
3. 반응에는 가시적 인 변화가 수반 될 수있다 :
* 색상 변화 : 솔루션은 색상이 변할 수 있으며, 새로운 화합물이 형성되었음을 나타냅니다.
* 가스 생산 : 기포가 형성되어 가스의 방출을 나타낼 수 있습니다.
* 침전물 형성 : 고체는 용기의 바닥에 형성되고 침전 될 수 있으며, 불용성 생성물의 형성을 나타냅니다.
* 열 방출 : 용액은 따뜻해 질 수 있으며, 발열 반응을 나타냅니다.
추가 분석 :
반응의 정확한 특성을 결정하려면 추가 정보가 필요합니다.
* 금속을 식별 : 다른 금속마다 반응성이 다르며 동일한 용액과 다르게 반응합니다.
* 솔루션을 식별하십시오 : 용액의 조성을 알면 특정 산화제 및 반응 생성물을 결정하는 데 도움이됩니다.
* 반응 조건을 관찰하십시오 : 온도, 압력 및 다른 물질의 존재는 반응에 영향을 줄 수 있습니다.
예 :
염산 (HCL)에 아연 (Zn)을 배치하면 기포가 형성되면 (수소 가스 방출) 아연이 용해됩니다. 이는 HCL 용액이 아연과 반응 할 수있는 산화제를 함유하고 아연은 수소보다 반응성이 있음을 나타냅니다.
중요한 참고 : 금속과 용액 사이의 반응은 위험 할 수 있습니다. 항상주의해서 처리하고 적절한 안전 절차를 따르십시오.