설명 :
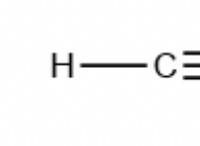
* 질소 (NIT) 두 질소 원자 사이에 트리플 결합이있는 동맥 핵 규조토 분자입니다. 이 트리플 결합은 매우 강하기 때문에 전자를 파괴하고 제거하기 위해 많은 양의 에너지가 필요합니다.
* 산화 질소 (NO) 질소와 산소 원자 사이에 이중 결합을 갖는 이종 핵 규조 분자이다. NO의 결합은 NIT의 트리플 결합보다 약합니다.
이온화 에너지에 영향을 미치는 요인 :
* 결합 강도 : 더 강한 결합은 파손되기 위해 더 많은 에너지가 필요하므로 이온화 에너지가 높아집니다.
* 전기 음성 : 원자가 전기 음성이 높을수록 전자가 더 단단히 고정되어 전자를 제거하기가 더 어려워집니다.
n₂ 및 no의 경우 :
* n trip은 NO에서 이중 결합보다 더 강한 트리플 본드를 갖습니다.
* 질소는 산소보다 전기 음성입니다.
따라서, N₂는 NO보다 더 높은 이온화 에너지를 갖는다.