1. 극성과 매력 :
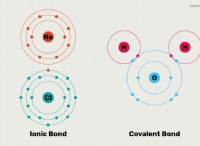
* 물 (HATER)은 극성 분자입니다 : 산소 원자는 약간 음전하를 가지며, 수소 원자는 약간 양의 전하를 갖는다. 이것은 쌍극자 순간을 만듭니다.
* 염화나트륨 (NaCl)은 이온 성 화합물입니다 : 나트륨 (Na+) 이온은 양으로 하전되고 염화물 (Cl-) 이온은 음으로 하전된다.
2. 해리 :
* 물 분자는 소금 결정을 둘러싸고 있습니다 : 물 분자 (수소 원자)의 양의 말단은 음으로 하전 된 염화물 이온에 끌리며, 물 분자 (산소 원자)의 음성 말단은 양으로 하전 된 나트륨 이온에 끌린다.
* 이 관광 명소 이로 인해 결정이 분리되어 개별 나트륨과 클로라이드 이온으로 분리됩니다.
3. 수화 :
* 분리 된 이온은 물 분자로 둘러싸여있다 : 이 물 분자는 각 이온 주위에 수화 쉘을 형성하여 서로를 효과적으로 분리하여 재조합을 방지합니다.
4. 솔루션 형성 :
* 용해 된 이온은 이제 물 전체에 균등하게 분산됩니다. 소금 결정은 더 이상 보이지 않으며 용액은 "포화"라고합니다.
키 포인트 :
* 용해는 화학적 변화가 아니라 신체적 변화입니다. 소금 이온은 여전히 물 분자로 둘러싸여 있습니다.
* 물에서 소금의 용해도는 제한적입니다. 소금을 너무 많이 넣으면 모든 용해는 아니며 일부는 용기 바닥에 고체로 유지됩니다.
시각화 :
작은 자석과 같은 물 분자가 소금 결정에서 하전 된 이온을 분리한다고 상상해보십시오. 물 분자는 이온에 "잡아"물을 분리하고 분산시킨다.