화학에서, "비금속"이라는 용어는 금속 특성이없는 원소와 화합물을 나타냅니다. 118 개의 알려진 요소 중 17 개만 구성했지만 비금속은 우리가 알고있는 삶에 필수적인 가장 중요한 요소 중 일부입니다. 비금속의 예는 탄소, 산소, 질소 및 수소; 이 모든 것은 유기 화합물의 기본 빌딩 블록입니다.
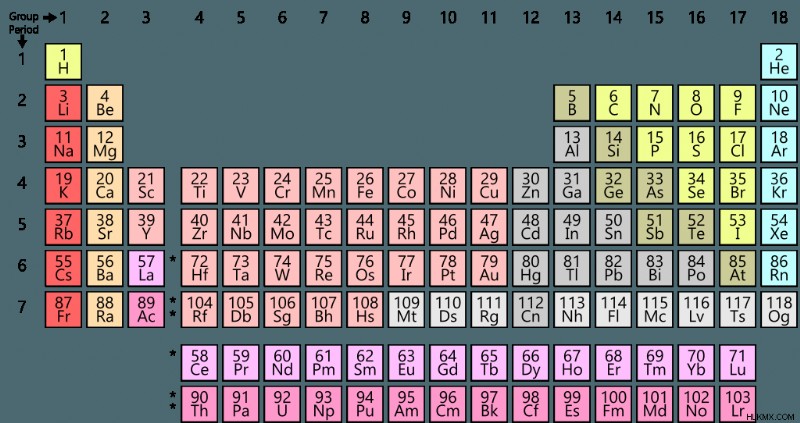
금속과 비교하여 비금속은 원자력 및 화학적 거동 측면에서 매우 가변적 인 특성 범위를 나타냅니다. 이는 비금속이 원 자간 및 분자간 결합 강도에서 크게 다르기 때문입니다. 대부분의 비금속은 표준 온도와 압력에서 가스 인 경향이 있으며 밀도가 낮습니다. 모든 비금속은 원소의 p- 블록 (수소 제외)의 주기성 테이블의 오른쪽에 위치합니다. 비금속에서 일반적으로 볼 수있는 속성은 다음과 같습니다.
- 이온/공유 결합의 경우
- 부서지기 쉬운
- 낮은 용융/비등 지점
- 높은 이온화 에너지 및 전기성
- 열과 전기의 가난한 도체
이 속성 목록은 필수적이거나 철저하지 않습니다. 일부 비금속에는 이러한 속성이 모두 있으며 일부는 거의 없습니다. 예를 들어 흑연은 전기 도체가 매우 우수하고 전자 장치에 사용되는 비금속 화합물입니다. 플라스틱과 같은 중합체는 가단성이 있고 형성 될 수있는 분자의 공유 결합 사슬입니다.
비금속의 종류
일반적으로 비금속은 두 가지 범주로 나뉩니다 : 반응성 비금속 및 할로겐 . 반응성 비금속은 물리적 및 화학적 특성에서 더 많은 변화를 나타내는 경향이 있습니다. 탄소 및 황과 같은 일부는 실온에서 고체이며 전기 음성이 적습니다. 산소와 같은 다른 사람들은 실온에서 가스이며 매우 전기 음성입니다. 반응성 비금속에는 또한 halogens (주기성 테이블의 그룹 17) 요소가 포함됩니다. 모든 할로겐은 7 개의 전자의 원자가 껍질을 가지므로 극도로 반응성이 높고 부정적인 이온을 쉽게 형성합니다. 다른 반응성 비금속은 다음과 같습니다.
- 수소 (H)
- 탄소 (C)
- 질소 (N)
- 산소 (O)
- 인 (P)
- 황 (s)
- 셀레늄 (SE)
할로겐은 다음과 같습니다.
- 불소 (F)
- 염소 (CL)
- Bromine (B)
- 요오드 (I)
- 아스타틴 (AS)
대조적으로, 고귀한 가스는 불활성 화학적 거동으로 특징 지어집니다. 고귀한 가스는 8 개의 전자의 전체 원자가 쉘을 가지므로 매우 안정적인 전자 구성에 존재합니다. 따라서, 고귀한 가스는 일반적으로 화합물을 형성하기 위해 다른 원소와 반응하지 않습니다. 고귀한 가스는 다음과 같습니다.
- 헬륨 (HE)
- 네온 (NE)
- 아르곤 (AR)
- 크립톤 (KR)
- Xenon (xe)
- Radon (RN)
- 요소 118 (Oganesson Og)
5 비금속 특성
1. 공유/이온 결합을 형성합니다
비금속의 주요 특성 중 하나는 공유 및 이온 결합을 만들어 화학 화합물을 형성한다는 것입니다. 공유 결합에서, 두 개의 원소는 완전한 쉘을 가질 때까지 원자가 전자를 공유합니다. 일반적인 일상적인 공유 화합물에는 이산화탄소, 에탄올 (알코올), 포도당 및 탄소 테트라 클로라이드가 포함됩니다. 공유 화합물의 요소는 각각 안정적인 전자 구성을 달성 할 수 있도록 전자를 공유합니다. 공유 화합물은 분자 형상에서 가장 큰 변화를 나타내는 경향이 있습니다. 공유 화합물은 전자 쌍 사이의 정전기 반발량을 최소화하는 형태를 취할 것이다. 공유 결합은 일반적으로 두 비금속 사이에 형성됩니다.
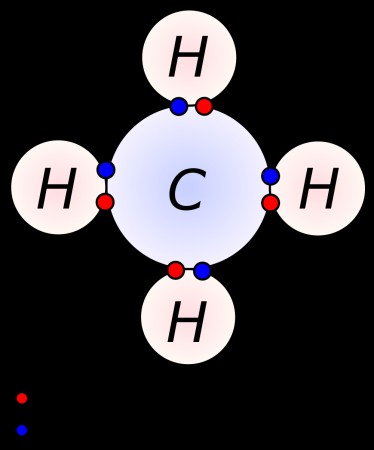
대조적으로, 이온 결합은 비금속과 금속 사이에 형성되는 경향이있다. 이온 결합에서, 한 요소는 다른 요소로부터 전자를 가져와 양이온과 음이온을 생성합니다. 반대로 하전 된 이온은 서로를 끌어 들이고 함께 뭉쳐 이온 성 화합물을 형성합니다. 일반적인 이온 성 화합물에는 테이블 소금, 탄산염, 황산염 및 염화 칼륨이 포함됩니다. 이온적 결합은 전기성에서 크게 다른 원소들 사이에 형성되는 경향이있다 (ΔEN> 2.0). 대부분의 이온 성 화합물은 격자로 알려진 이온의주기적인 구조로 자신을 배치합니다.
2. 취성
비금속으로 제조 된 대부분의 화합물 공유 및 이온 성 화합물은 부서지기 쉬운 경향이 있으며 충분한 힘이 적용되면 산산이 부서집니다. 금속과 달리 비금속 화합물은 가단성과 연성이 아닙니다. 대부분의 비금속 화합물은 깨지지 않고 특정 지점을 지나서 변형 될 수 없으며 성형 할 때 강도를 잃게됩니다.

비금속 화합물은 이온 성 및 공유 결합의 특성으로 인해 부서지기 쉬운 경향이 있습니다. 이온 성 및 공유 결합은 전자의 공유/포획을 포함한다. 두 종류의 화합물은 정전기 반발을 최소화하는 방식으로 자신을 배열합니다. 예를 들어, 이온 성 화합물에서, 양성 및 음성 원자는 음이온에 정렬 된 양의 이온을 갖는 단단한 결정 구조에 제자리에 고정된다. 힘을 적용하면 이온의 정렬을 이동시켜 양성이 부정적인 양성 및 부정과 일치 할 수 있습니다. 반발은 화합물이 골절되게한다.
마찬가지로, 공유 결합은 전자와 원자가 특정 방식으로 배열되어야한다. 기계적 힘의 적용은 화합물을 파괴하게하는 배열을 방해한다. 대조적으로, 금속 결합은 비편성 전자 결합으로 인해 서로 이동하고 미끄러질 수 있습니다. 이것이 금속이 연성과 가단성이있는 이유이며, 화학적 결합을 깨지 않고 원자 구조를 바꿀 수 있습니다.
.3. 낮은 용융/비등 지점
모든 비금속 화합물이 낮은 융점과 끓는점을 갖는 것은 사실이 아닙니다. 예를 들어, 소금은 801 ° C의 용융점이 매우 높습니다. 그러나 금속과 비교하여 비금속 화합물은 비교적 녹는 융점을 갖습니다. 녹는 점과 끓는 점은 왜 대부분의 비금속이 실온에서 기상 인 이유를 설명합니다.
비금속 화합물, 구체적으로 공유 화합물은 상대적으로 약한 분자간 상호 작용으로 인해 녹는 점과 비등점이 낮습니다. 물질의 상 거동은 분자간 결합의 강도에 의해 결정됩니다. 금속은 분자간 매력이 매우 강하기 때문에 녹는 점과 비등점이 매우 높습니다. 반면에 공유 화합물은 강한 분자간 관광 명소를 가지고 있지 않습니다. 이것은 대부분의 공유 분자가 전기적으로 중립적이므로 적어도 금속이하는 정도가 아니라 이웃을 유치하지 않기 때문입니다.
이온 성 화합물은 공유 화합물보다 더 높은 용융/끓는점을 가지지 만 여전히 금속의 것보다 적습니다. 이온 성 화합물을 가열하면 입자의 운동 에너지가 증가합니다. 특정 임계 값 외에도 운동 에너지는 정전기 인력을 극복하고 격자 구조가 분리됩니다. 대조적으로, 금속은 원자가 화학 결합을 깨지 않고 장소를 이동할 수 있기 때문에 녹는 지점이 매우 높다.
4. 높은 이온화 에너지/전기성
비금속은 높은 이온화 에너지를 갖는 경향이 있습니다. 이것은 비금속 원자에서 전자를 제거하기가 어렵다는 것을 의미합니다. 비금속은 이온화 에너지가 높기 때문에 전자 쉘이 얼마나 큰지에 비해 핵이 얼마나 크기 때문에. 산소 및 불소와 같은 크고 양으로 하전 된 원자의 핵은 전자를 매우 강하게 끌어 당겨 제거하기가 어렵습니다.
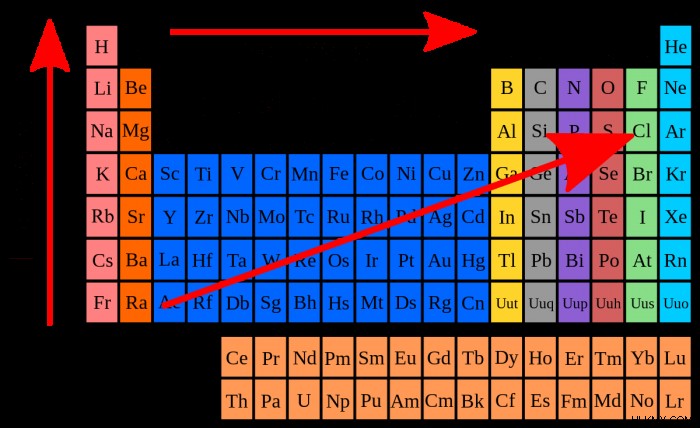
같은 이유는 왜 비금속이 금속보다 전기 음성 인 경향이 있는지 설명합니다. 비금속의 긍정적으로 하전 된 핵은 전자를 강하게 당기는데, 때로는 이웃 원자에서 그들을 제거 할 수있을 정도로 강합니다. 일반적으로, 왼쪽 왼쪽은 주기율표에 걸쳐 더 높은 이온화 에너지와 전기성이 발생합니다.
5. 열과 전기의 가난한 도체
비금속은 또한 열과 전기의 도체가 상대적으로 열악한 경향이 있지만 일부 예외는 존재합니다. 비금속이 열악한 전도체 인 이유는 금속이 비교적 좋은 도체 인 이유와 관련이 있습니다. 금속은 결합을 깨지 않고 많은 운동 에너지를 흡수 할 수 있기 때문에 열을 잘 수행합니다. 대조적으로 비금속은 안정적으로 유지하기 위해 고정 된 원자 배열이 필요하므로 너무 많은 운동 에너지가 그들의 결합을 극복 할 것입니다. 금속은 전자가 이동할 수있는 수많은 열린 궤도가 있기 때문에 전기 도체가 우수합니다. 비금속은 궤도가 완전한 경향이 있으므로 전자는 전압에 도입 될 때 갈 곳이 없습니다.
수소의 호기심 :금속 또는 비 금속?
일반적으로, 최초의 요소 수소는 비금속으로 분류됩니다. 그러나, 수소는 매우 독특한 특성을 가지고있어 금속 또는 비금속으로 분류하기가 어렵습니다. 예를 들어, 수소는 공유 결합에 관여하며 비금속과 같은 가스로 자연적으로 존재합니다. 그러나, 수소는 또한 단일 전자를 쉽게 흘려서 금속에서 볼 수있는 긍정적으로 하전 된 이온을 형성한다. 수소의 독특한 특성 믹스 특성은 매우 간단한 원자 구조의 결과입니다.
1935 년에 물리학 자 Eugene Wigner와 Hillard Huntington은 매우 높은 온도와 압력에서 수소가 금속 액체 또는 고체에 응축 될 것이라고 예측했습니다. 이 이국적인 수소 단계는 금속처럼 행동하고 열과 전기의 매우 우수한 도체가 될 것으로 예상됩니다. 현재, 수소는 기체 상태에서만 존재하는 것으로 관찰되었지만, 액체 금속 수소는 목성이나 토성과 같은 가스 거대 행성의 코어에 존재할 수 있다고 믿어집니다. 액체 금속 수소의 조밀 한 코어는 고전적인 예측과 상충되는 가스 거인의 매우 강력한 자기장을 설명 할 것입니다.
요약하면, 비금속은 금속 특성의 부족으로 특징 지어지는 화학 물질입니다. 비금속은 일반적으로 실온에서 기상 또는 액체이며 반응성 비금속과 고귀한 가스로 나뉩니다. 비금속은 공유 결합에 관여하고, 부서지기 쉬운 연약한 화합물을 형성하며, 녹는/끓는점이 낮고, 이온화 에너지가 높고 전기성이 있으며 전기 도체가 열악합니다. 비금속은 비교적 넓은 원자 핵 크기와 전자 구성으로 인해 금속보다 화학적으로 가변적입니다. 모든 비금속은주기 테이블의 p- 블록에 있습니다.