Diborane은 유기 화합물이며 화학적으로 B2 H6으로 작성됩니다. 디포 란 분자에는 4- 말단 붕소-하이드로겐 결합 및 2 개의 브리지 붕소-하이드로겐-붕어가 존재한다. 그것은 달콤한 냄새가 있으며 정상적인 실내 온도에서 기체 상태에 존재합니다. 염증성이 있고 독성이 높으므로 인간 건강에는 지속 가능하지 않습니다. 디보 레인은 환경에 자연적으로 존재하지 않지만 실험실 또는 산업 방법에 의해 준비되어 있습니다. 디보 레인의 끓는 지점은 염증성 특성으로 인해 매우 낮습니다. 디보란 분자에는 이온 결합뿐만 아니라 공유 결합이 존재한다.
구조
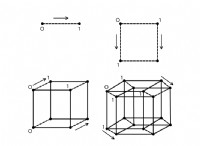
디보 레인 구조의 대칭은 B2 H6입니다. 히드 라이드 중 4 개는 말단이고, 다른 두 개는 붕소 중심 사이의 연결로 작용합니다. B-H 브리지 본드 및 B-H 터미널의 암스트롱 값은 각각 1.33 및 1.19입니다. 결합 길이의 차이는 그들의 다른 강점을 반영하며, B-H 결합은 둘 중 약한 것입니다.
적외선 스펙트럼에서 B-H 터미널 및 B-H 결합의 진동 구조는 약 2100 및 2500cm이며, 이들의 취약성을 나타낸다. 붕소와 말기 수소 원자 사이의 연결은 분자 측정 이론에 의해 2 개의 중심과 2- 전자 공유 결합으로 정의됩니다.
그러나, 탄화수소와 같은 화합물과는 달리, 브리징 수소 원자와 붕소 원자 사이의 결합은 뚜렷하다. 각 붕소는 말기 수소 원자에 연결하기 위해 2 개의 전자가 필요하며 추가 결합을 위해 하나의 원자가 전자가 남았습니다. 브리징 수소 원자 각각은 하나의 전자를 기여합니다. 바나나 채권은 이러한 종류의 채권으로 구성됩니다.
Diborane의 사용 및 응용
- 1960 년대에 디보 레인 (B2 H6)은 우주선 프로젝트의 연료로 사용되었다. 디보 레인은 저 분자 질량과는 별도로 약간의 저장된 에너지를 가지고 있다고 생각되었다. .
- Diborane (B2 H6)은 인기있는 시약으로 사용되기 때문에 수경 화학 과정에 사용되며, 마르코프나 코코프 방지 제품을 주로 제공하고 있습니다.
- 탄화수소의 중합 공정에서, 디보 레인 (B2 H6)은 촉매로 사용되며, 이는 반응에 디보 레인이 존재하며 전체 과정에서 반응하지 않고 중합 반응 속도를 증가시키는 데 도움이된다. .
- 반도체의 제조에서 Diborane (B2 H6)은 도핑 제로서 사용되며, 즉, 원래 화학 물질에 추가 된 불순물로 사용된다. 이로 인해 전기 및 자기 특성의 어느 정도를 나타냅니다.
- Diborane (B2 H6)은 반도체 준비에 불꽃 속도 가속기로도 사용됩니다.
- 반도체의 제조 방법 동안 순수한 붕소가 생성 될 때, 우리는 중간 종으로 디보 레인 (B2 H6)을 얻을 수 있습니다.
- Diborane (B2 H6)은 플라즈마에서 중금속의 불순물을 줄이기 위해 Tokamak 기계 벽의 코팅 시약으로 사용됩니다. Tokamak의 기계는 자기장을 사용하여 혈장을 제한하기 위해 핵 융합 연구 과정에 사용되는 장치입니다.
- Diborane (B2 H6)은 중합 공정 및 고무 호스, 신발 발바닥, 장난감, 지우개, 충격 흡수기, 컨베이어 벨트 등과 같은 다양한 물체에서 고무 불카기로 사용됩니다.
- Diborane (B2 H6)은 또한 많은 화학 반응에서 환원제로 사용되며,이 자체는 수소를 제공함으로써 주어진 반응물을 감소시키기 위해 산화됩니다. 디보 레인은 카르복실산을 각각의 알코올로 효율적으로 감소시킨다.
결론
Diborane은 화학 및 과학 생활에서 몇 가지 용도로 사용됩니다. 주어진 반응물을 감소시키기 위해 많은 화학 반응에서 환원제로 사용되었다; 중합 공정에서 촉매 및 반도체 형성 중에 사용됩니다.