다음은 요소 요금 차트와 요소를 모르는 경우 요소의 청구를 찾는 방법에 대한 설명입니다. 전하, 산화 상태 및 원자가의 차이도 설명됩니다. 참조를 위해이 그래픽과 테이블을 다운로드하여 인쇄 할 수 있습니다.
요소의 청구를 찾는 방법
요소의 책임을 찾는 4 가지 방법이 있습니다.
- 주기적인 테이블을 사용하십시오. 요소의 일반적인 요금은 그룹에 공통적입니다.
그룹 1 (알칼리 금속) :1+
그룹 2 (알칼리성 지구 금속) :2+
그룹 3-12 (전이 금속) :가변 양수
Lanthanide 및 Actinide 시리즈 :가변 양수
그룹 13 :3+
그룹 14 :4+ 또는 4-
그룹 15 :3-
그룹 16 :2-
그룹 17 (할로겐) :1-
그룹 18 (고귀한 가스) :0
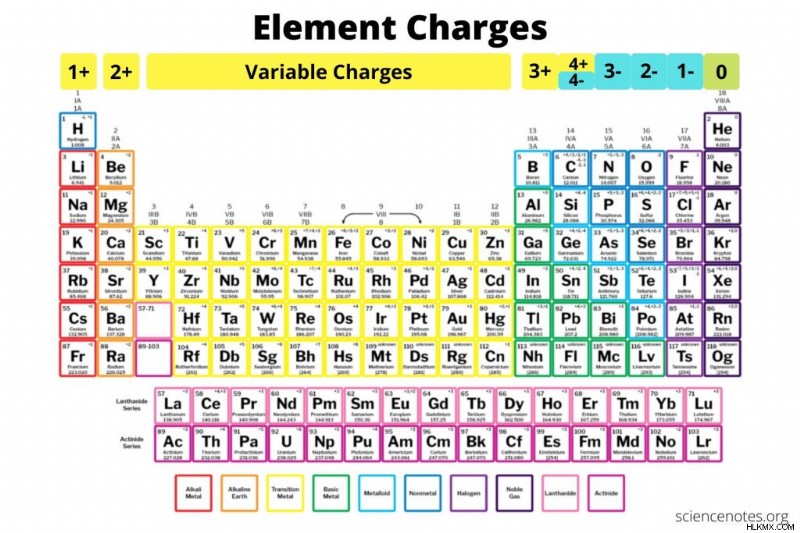
- 차트를 사용하십시오. 차트는 요소의 실제 동작에 대한 경험적 데이터에서 나오며, 이는 주기율표 예측과 다를 수 있습니다. 다음은 두 차트입니다. 첫 번째는 공통 요소 전하를 보여주고, 두 번째는 첫 45 개의 요소에 대한 모든 요소 전하 (대담한 가장 일반적인 전하)를 보여줍니다.
- 단일 원자의 경우 전하는 전자 수를 뺀 양성자 수입니다.
- 화합물의 충전 균형을 잡음으로써 충전을 찾으십시오.
| 번호 | 요소 | 충전 |
|---|---|---|
| 1 | 수소 | 1+ |
| 2 | 헬륨 | 0 |
| 3 | 리튬 | 1+ |
| 4 | 베릴륨 | 2+ |
| 5 | 붕소 | 3-, 3+ |
| 6 | 탄소 | 4+ |
| 7 | 질소 | 3- |
| 8 | 산소 | 2- |
| 9 | 불소 | 1- |
| 10 | 네온 | 0 |
| 11 | 나트륨 | 1+ |
| 12 | 마그네슘 | 2+ |
| 13 | 알루미늄 | 3+ |
| 14 | 실리콘 | 4+, 4- |
| 15 | 인 | 5+, 3+, 3- |
| 16 | 황 | 2-, 2+, 4+, 6+ |
| 17 | 염소 | 1- |
| 18 | 아르곤 | 0 |
| 19 | 칼륨 | 1+ |
| 20 | 칼슘 | 2+ |
| 21 | 스칸디움 | 3+ |
| 22 | 티타늄 | 4+, 3+ |
| 23 | Vanadium | 2+, 3+, 4+, 5+ |
| 24 | 크롬 | 2+, 3+, 6+ |
| 25 | 망간 | 2+, 4+, 7+ |
| 26 | 철 | 2+, 3+ |
| 27 | 코발트 | 2+, 3+ |
| 28 | 니켈 | 2+ |
| 29 | 구리 | 1+, 2+ |
| 30 | 아연 | 2+ |
| 31 | 갈륨 | 3+ |
| 32 | 게르마늄 | 4-, 2+, 4+ |
| 33 | arsenic | 3-, 3+, 5+ |
| 34 | 셀레늄 | 2-, 4+, 6+ |
| 35 | Bromine | 1-, 1+, 5+ |
| 36 | 크립톤 | 0 |
| 37 | Rubidium | 1+ |
| 38 | strontium | 2+ |
| 39 | yttrium | 3+ |
| 40 | 지르코늄 | 4+ |
| 41 | niobium | 3+, 5+ |
| 42 | Molybdenum | 3+, 6+ |
| 43 | Technetium | 6+ |
| 44 | Ruthenium | 3+, 4+, 8+ |
| 45 | Rhodium | 4+ |
| 46 | Palladium | 2+, 4+ |
| 47 | 은 | 1+ |
| 48 | 카드뮴 | 2+ |
| 49 | indium | 3+ |
| 50 | tin | 2+, 4+ |
| 51 | 안티몬 | 3-, 3+, 5+ |
| 52 | 텔루 리움 | 2-, 4+, 6+ |
| 53 | 요오드 | 1- |
| 54 | Xenon | 0 |
| 55 | 세움 | 1+ |
| 56 | 바륨 | 2+ |
| 57 | 란타늄 | 3+ |
| 58 | Cerium | 3+, 4+ |
| 59 | praseodymium | 3+ |
| 60 | Neodymium | 3+, 4+ |
| 61 | promethium | 3+ |
| 62 | 사마 리움 | 3+ |
| 63 | Europium | 3+ |
| 64 | 가돌리늄 | 3+ |
| 65 | Terbium | 3+, 4+ |
| 66 | dysprosium | 3+ |
| 67 | holmium | 3+ |
| 68 | erbium | 3+ |
| 69 | thulium | 3+ |
| 70 | ytterbium | 3+ |
| 71 | lutetium | 3+ |
| 72 | hafnium | 4+ |
| 73 | tantalum | 5+ |
| 74 | 텅스텐 | 6+ |
| 75 | rhenium | 2+, 4+, 6+, 7+ |
| 76 | osmium | 3+, 4+, 6+, 8+ |
| 77 | iridium | 3+, 4+, 6+ |
| 78 | 플래티넘 | 2+, 4+, 6+ |
| 79 | 골드 | 1+, 2+, 3+ |
| 80 | 머큐리 | 1+, 2+ |
| 81 | 탈 리움 | 1+, 3+ |
| 82 | 리드 | 2+, 4+ |
| 83 | Bismuth | 3+ |
| 84 | 폴로늄 | 2+, 4+ |
| 85 | 아스타틴 | ? |
| 86 | 라돈 | 0 |
| 87 | Francium | ? |
| 88 | 라듐 | 2+ |
| 89 | actinium | 3+ |
| 90 | Thorium | 4+ |
| 91 | protactinium | 5+ |
| 92 | 우라늄 | 3+, 4+, 6+ |