화학에서 요소 원자 핵에서 모두 같은 수의 양성자를 갖는 원자로 구성된 순수한 물질로 정의된다. 다시 말해, 요소의 모든 원자는 동일한 원자 번호를 갖는다. 요소의 원자 (때로는 "화학 요소"라고도 함)는 화학적 수단에 의해 작은 입자로 나눌 수 없습니다. 원소는 원자 입자로만 나뉘어 또는 원자력에 의해 다른 원소로 변형 될 수 있습니다. 현재 118 개의 알려진 요소가 있습니다.
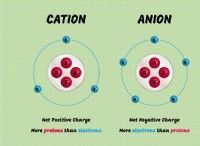
원소의 원자가 전하를 전하하면 이온이라고합니다. 다른 수의 중성자를 가진 원소의 원자를 동위 원소라고합니다. 때로는 동위 원소도 자신의 이름을 가지고 있지만 여전히 요소의 예입니다. 예를 들어, 양성자, 중수소 및 삼중 수소는 모두 원소 수소의 동위 원소입니다. 요소는 Allotropes라는 다른 형태를 취할 수 있지만 화학적 동일성을 바꾸지는 않습니다. 예 :다이아몬드와 흑연 모두 순수한 원소 탄소입니다.
요소의 예
주기율표의 118 개 요소 중 하나는 모든 요소의 예입니다. 원소는 양성자의 수에 의해 정의되기 때문에, 한 유형의 원자로 구성된 임의의 동위 원소, 이온 또는 분자도 원소의 예이다. 그러나 요소의 예를 지정하도록 요청받은 경우 안전을 재생하고 동위 원소, 분자 또는 동위 원소가 아닌주기적인 테이블에 요소를 나열하십시오.
.- 수소 (원자 번호 1; 요소 기호 H)
- 헬륨 (원자 번호 2, 요소 기호 HE)
- 철 (원자 번호 26; 요소 기호 Fe)
- 네온 (원자 번호 10; 요소 기호 NE)
- 탄소 -12 및 탄소 14 (6 개의 양성자이지만 중성자 수가 다른 2 개의 탄소)
- 산소 가스 (O 2 ; o 3 여기에는 특별한 오존의 이름이 있습니다)
- 삼중 수소 (수소의 동위 원소)
- 다이아몬드, 흑연 및 그래 핀 (탄소 동종)
요소의 분자는 화학 반응을 통해 작은 조각으로 나눌 수 있습니다. 그러나 원자의 원소 정체성은 변하지 않고 남아있다.
요소가 아닌 물질의 예
물질에 둘 이상의 유형의 원자가 포함 된 경우 요소가 아닙니다. 허구의 요소는 실제 화학 요소가 아닙니다. 요소가 아닌 물질의 예는 다음과 같습니다.
- 물 (H 2 O, 수소 및 산소 원자로 구성)
- 강철 (철, 니켈 및 기타 요소로 구성)
- 황동 (구리, 아연 및 기타 요소로 구성)
- 공기 (질소, 산소 및 기타 요소로 구성)
- 전자
- 중성자
- 플라스틱
- 창
- 고양이
- 크립토나이트
- Divinium
- unobtainium
요소 이름, 기호 및 원자 번호
개별 요소를 참조하는 세 가지 방법이 있습니다. 각 요소에는 이름, 요소 기호 및 원자 번호가 있습니다. IUPAC (International Union of Pure and Applied Chemistry)는 표준 이름과 기호를 승인하지만 개별 국가 내에서 다른 요소 이름이 사용될 수 있습니다.
일부 요소 이름은 역사적이지만 대부분은 그들을 발견 한 사람이나 그룹에 의해 지명되었습니다. 요소 이름은 일반적으로 사람 (실제 또는 신화), 장소 (실제 또는 신화) 또는 미네랄을 참조합니다. 많은 요소 이름이 -ium 접미사로 끝나지 만 할로겐 이름은 -ine 결말을 가지고 있으며 고귀한 가스는 결말을 가지고 있습니다. 요소 이름은 해당 요소의 단일 원자 또는 이온, 동위 원소 또는 해당 요소로만 구성된 분자를 나타냅니다. 예를 들어, 산소는 단일 산소 원자, 산소 가스 (O 2 를 가리킬 수 있습니다. 또는 o 3 ) 또는 동위 원소 산소 -18.
각 요소에는 고유 한 1 또는 2 글자 기호가 있습니다. 상징의 예로는 수소의 H, 칼슘의 경우 CA 및 Oganesson의 OG가 포함됩니다.
주기율표는 원자 번호가 증가하는 순서대로 요소를 나열합니다. 원자 번호는 해당 요소의 원자에서 양성자 수입니다. 원자 수의 예로는 수소의 경우 1, 헬륨 2 개, 탄소의 경우 6이 포함됩니다.
요소, 분자 및 화합물
요소는 한 가지 유형의 원자로 구성됩니다. 분자 화학적 결합에 의해 함께 연결된 둘 이상의 원자로 구성됩니다. 일부 분자는 h 2 와 같은 요소의 예입니다 , n 2 및 O. a 화합물 둘 이상의 다른 다른 로 구성된 분자 유형입니다. 원자는 화학 결합에 의해 결합된다. 모든 화합물은 분자이지만 모든 분자가 화합물이 아닙니다.
참고 :IUPAC는 분자와 화합물을 구별하지 않아 화학 결합을 공유하는 둘 이상의 원자의 고정 비율로 형성된 순수한 물질로 정의합니다. 이 정의에 의해, o 2 요소, 분자 및 화합물 일 것입니다. 정의가 다르기 때문에 화학 교사는 아마도 요소/화합물에 대한 질문을 피하고 단순히 주기적 테이블의 118 요소에 요소의 예로 집중해야 할 것입니다.
.참조
- Burbidge, E.M.; et al. (1957). "별의 요소의 합성". 현대 물리학의 리뷰 . 29 (4) :547–650. doi :10.1103/Revmodphys.29.547
- Earnshaw, A.; Greenwood, N. (1997). 요소의 화학 (제 2 판). Butterworth-Heinemann.
- iupac (1997). "화학 요소". 화학 용어의 개요 (제 2 판) (“골드 북”). 블랙웰 과학 간행물. doi :10.1351/Goldbook
- Myers, Rollie J. (2012). “요소와 화합물이란 무엇입니까?”. j. 화학 Educ. 89 (7) :832–833. doi :10.1021/ed200269e