
중수소는 원자 핵에 하나의 양성자와 하나의 중성자를 갖는 수소 동위 원소입니다. 대조적으로, 대부분의 수소는 양성자와 중성자가없는 양성자라고 불리는 동위 원소입니다. 다음은 방사성, 역사, 용도 및 출처를 포함한 중수소 사실 모음입니다.
중수소 방사성인가?
양성자와 같은 중수소는 안정적인 동위 원소입니다. 다시 말해, 그것은 입니다 방사성. 유일한 방사성 수소 동위 원소는 삼중습입니다.
역사
과학자들은 중수소가 발견되기 전에 안정적인 동위 원소를 알고 있었지만, 수소는 동위 원소를 가질 수 있다고 생각하지 않았습니다. 그 이유는 중성자가 아직 발견되지 않았기 때문에 연구원들은 동위 원소가 양성자 수와 핵 전자라고 불리는 것과 다르다고 생각했습니다. 이러한 추론에 의해, 핵은 하나의 양성자 만 함유 할 수 있기 때문에 수소는 동위 원소를 가질 수 없었다. 따라서 중수소 (및 삼중습)의 발견은 약간의 충격으로 왔으며 동위 원소에 대한 이해를 완전히 변화 시켰습니다.
Harold Urey는 1931 년에 중수소를 발견했습니다. 그와 그의 공동 작업자 인 Ferdinand Brickwedde는 Washington, D.C의 National Bureau of Standards의 저온 물리 실험실을 사용하여 액체 수소로부터 동위 원소를 증류시켰다. 화학.
명명
수소 요소는 각 동위 원소의 이름을 가지고 있다는 점에서 독특합니다. 중수소는 그리스어 단어에서 이름을 얻습니다 , 이는 - ium 과 결합 된“두 번째”를 의미합니다 요소의 접미사. 이름은 핵의 두 번째 핵을 나타냅니다.
Urey는 Protium, 중수소 및 삼중습을 지명했습니다. 동위 원소의 발견 자로서, 이것은 그의 권리였습니다. 그러나 일부 과학자들은 그 이름에 저항했습니다. 예를 들어, 어니스트 러더 포드 (Ernest Rutherford)는 그리스어 diploos 에서 중수소가 "Diplogen"으로 지정되어야한다고 느꼈습니다. ("더블"). Rutherford는 중수소 핵을 "Deuteron"또는 "Deuton"이 아닌 "외교"라고 불렀습니다.
.중수소 특성
중수소는 몇 가지 흥미로운 특성을 나타냅니다.
- 중수소와 삼중 수소는 일반 수소 (Protium)보다 더 강한 화학적 결합을 형성합니다.
- 중수소는 일반 수소보다 트리플 포인트, 끓는점, 증기 압력, 융합 열 및 기화 열이 상당히 높습니다.
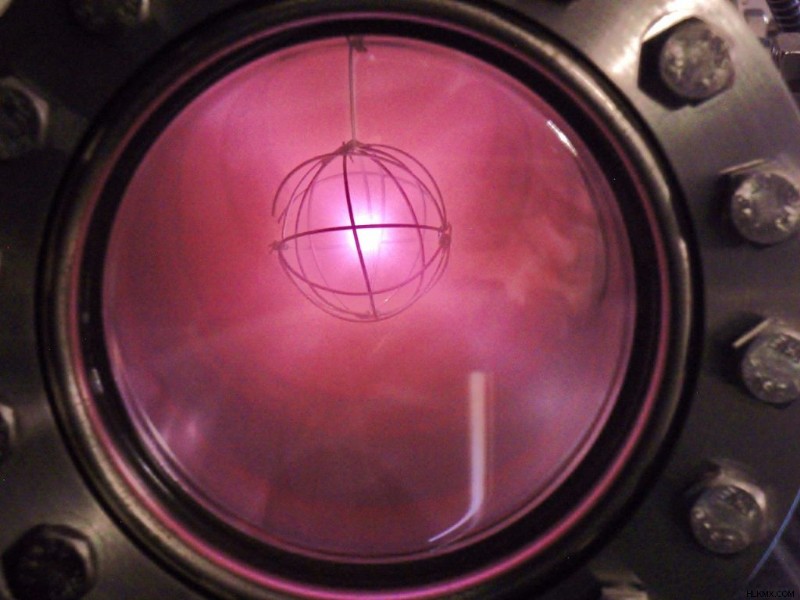
- 중수소 가스는 무색입니다. 그러나 이온화 될 때 특징적인 분홍색 빛을 방출합니다.
- 더 강한 본드는 무거운 물이 일반 물 (1.624 g/cm)보다 약 10.6 배 더 밀도가 높습니다. 무거운 물 얼음은 일반 물에 가라 앉지 만 무거운 물에 떠 다니고 있습니다.
- 무거운 물은 또한 평범한 물보다 점성이 더 높습니다. (300k에서 12.6 μpa · s).
더 많은 중수소 사실
- 중수소는 기호 D 또는 H로 표시됩니다. 때로는 중대한 수소라고도합니다.
- 중수소는 양성자보다 훨씬 덜 풍부합니다. 천연 수소의 0.0156%에 불과합니다.
- 중수소 핵을 수신 론 또는 도이튼이라고합니다.
- 중수소는 홀수의 양성자와 홀수의 중성자를 갖는 5 개의 안정적인 동위 원소 중 하나입니다. 일반적으로 이중 공동 원자는 불안정하고 베타 붕괴를 통해 겪습니다.
- 중수소는 태양계와 다른 별 내의 다른 행성에 존재합니다. 태양계의 가스 거인은 서로 거의 동일한 중수소 농도를 포함합니다.
- 중수소의 자연 풍부는 그 근원에 따라 다릅니다.
- 중수소 (예 :양성자)는 극도의 압력 하에서 액체 금속이됩니다.
- 신 부두통에 대한 반물질의 대응 물은 안티 프로 톤과 항 혈관으로 구성된 항 테르 론이다. 반물질 중수소는 항산공으로 불리며 항 침대 및 포지 트론으로 구성됩니다.
건강 영향
인간은 무거운 수소에 노출되지 않습니다 (d 2 ), 그러나 과학자들은 무거운 물의 영향에 대해 많은 것을 알고 있습니다 (d 2 o) 생물학적 시스템.
평범한 물에는 항상 미량의 중수소가 포함되어 있으므로 약간의 동위 원소를 섭취하는 것은 정상입니다. 실제로, 당신은 약간의 무거운 물을 마실 수 있습니다. 일부 의료 진단 검사에도 사용됩니다. 조류와 박테리아는 순수한 무거운 물 속에 살 수 있지만 더 천천히 자랍니다. 인간과 다른 동물은 심한 물이 체중의 약 20%를 차지할 때 물병 독성을 경험합니다. 결국, 무거운 물은 사망을 일으킬 정도로 충분한 유사 분열을 방해합니다. 무거운 물 독성이 건강한 세포보다 암 세포에 더 부정적인 영향을 미치는 것은 흥미 롭습니다.
그러나 중수 약물은 많은 잠재적 인 이점을 제공합니다. 중수소는 산화 손상으로부터 특정 영양소를 보호하는 데 도움이됩니다. 경구 폴리오 바이러스 백신과 같은 살아있는 백신을 안정화시킵니다. 중수 약물은 암 약물의 유전 독성을 감소시킵니다. 중수소는 일반 수소보다 탄소에 더 강하게 결합하기 때문에 중수 약물은 대사되기 전에 더 오래 지속될 수 있습니다. 중수소 길이주기 리듬 시계. 무거운 물은 감마 방사선으로부터 생쥐를 보호하는 것으로 나타났습니다.
중수소 사용
중수소에는 몇 가지 용도가 있습니다.
- 중수소는 헤비 워터 중재 핵분열 반응기에서 사용되는 것으로 보이며, 일반적으로 무거운 물이있어 중성자가 너무 많은 것을 흡수하지 않고 느리게합니다.
- 대부분의 퓨전 반응기 설계에는 중수소가 포함되며, 종종 삼중습이 포함됩니다.
- 핵 자기 공명 (NMR) 이미징은 신호를 쉽게 걸러 내기 때문에 중수소를 용매로 사용합니다.
- 중성자 산란 기술은 중수소를 사용하여 실험에서 산란 소음을 줄입니다.
- 중수소는 적외선 분광법 또는 질량 분석법을 사용하여 감지 할 수있는 안정적인 동위 원소 트레이서입니다.
- 중수 약물은 정상 수소를 사용하여 제조 된 약물과 다르게 작용하여 다양한 의학적 가능성을 제공합니다.
중수소 공급원
오늘날 발견 된 중수소의 대부분은 빅뱅 중에 형성되었습니다. 원자로를 사용하여 중수소를 만들 수는 있지만 비용 효율적이지는 않습니다. 따라서 대부분의 중수소는 일반 물에서 자연적으로 발생하는 중수를 분리하는 데 따릅니다.
참조
- 무기 화학 명칭에 관한 IUPAC위원회 (2001). “무오니늄과 수소 원자와 그 이온의 이름”. 순수하고 응용 화학 . 73 (2) :377–380. doi :10.1351/pac200173020377
- Kushner, D. J., Baker, A.; Dunstall, T. G. (1999). “무거운 물과 중수화 된 화합물의 약리학 적 용도 및 관점”. j Physiol Pharmacol . 77 (2) 79-88.
- Lide, D. R., ed. (2005). 화학 및 물리학의 CRC 핸드북 (86 번째 ed.). Boca Raton (FL) :CRC Press. ISBN 0-8493-0486-5.
- O'Leary, D. (2012 년 2 월). “중수소에 대한 행위”. 자연 화학 . 4 (3) :236. doi :10.1038/nchem.1273
- Sanderson, K. (2009 년 3 월). “무거운 약물에 대한 큰 관심”. 자연 . 458 (7236) :269. doi :10.1038/458269a







