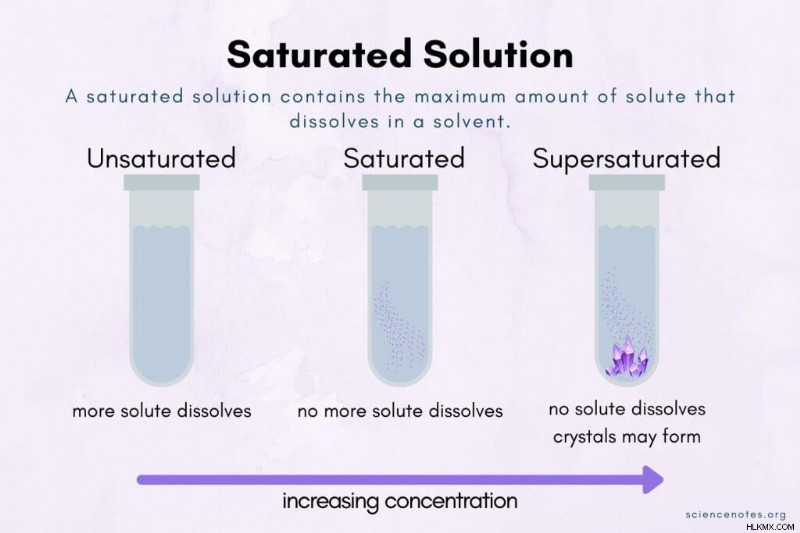
화학에서 포화 용액 용매에 용해 된 최대 용질의 양을 포함하는 화학 용액입니다. 포화 점 최대 농도의 지점입니다. 추가 용질은 포화 용액이나 포화 지점을 지나서 녹지 않습니다.
포화에 영향을 미치는 요소
용매에 용해되는 용질의 양은 여러 요인에 따라 다릅니다. 용해도에 영향을 미치는 주요 요인 중 일부는 다음과 같습니다.
- 온도 :온도가 증가하면 용해도가 증가합니다. 예를 들어, 더 많은 소금이 냉수보다 온수에 용해됩니다. 추운 온도에서의 포화 용액은 더 높은 온도에서 포화 용액보다 농도가 낮습니다.
- 압력 :압력 증가는 용액에 더 많은 용질을 강요합니다. 하나의 적용은 가스를 이산화탄소와 같은 액체에 소다로 용해시키는 것입니다.
- 화학 조성 :용질 및 용매의 특성은 용해도에 영향을 미칩니다. 용액의 다른 화합물의 현재도 마찬가지입니다. 예를 들어, 물 속의 소금보다 물에 더 많은 설탕을 녹일 수 있습니다.
- pH :솔루션의 산도 또는 염기성은 이온이 분리되는지 여부에 영향을 미치므로 용해도에 영향을 미칩니다.
포화 대 과포화 솔루션
이러한 요소를 제어하면 과포화가 가능합니다. 과포화 용액 용매에 용해시켜야하는 것보다 더 많은 용질을 함유하는 불안정한 용액입니다. 예를 들어, 온수로 설탕의 포화 용액을 준비한 다음 용액을 식히면 온도가 변할 때 과포화됩니다. 용액을 방해하거나 핵 생성 지점 (종자 결정 또는 용기의 스크래치와 같은)을 추가하면 결정 성장이 유발됩니다.
포화 솔루션의 예
포화 솔루션은 실험실뿐만 아니라 모든 수명에서 일반적입니다! 친숙한 예는 다음과 같습니다.
- 소다는 물에 이산화탄소의 포화 용액입니다. 용기를 열어 압력이 감소하면 이산화탄소의 용해도가 감소하고 용액에서 기포가 발생합니다.
- 용해가 멈출 때까지 커피 나 차에 설탕을 첨가하면 포화 용액이 형성됩니다.
- 녹은 버터에 소금을 첨가하여 곡물이 용해를 멈추는 지점까지 포화 용액을 형성합니다.
- 꿀은 물에 설탕 (포도당 및 과당)의 포화 용액입니다. 꿀을 냉장하면 온도를 낮추면 설탕 용해도가 낮아서 결정됩니다.
- 밀가루 코코아 혼합물이 물이나 우유에 섞는 것이 멈출 때까지 포화 용액을 형성합니다.
- 더 이상 녹을 때까지 가루 비누를 물에 넣어 포화 용액을 만들 수 있습니다.
포화 용액을 만드는 방법
포화 용액을 준비하는 방법에는 여러 가지가 있습니다.
- 더 이상 용해되지 않을 때까지 용매에 용질을 첨가하십시오.
- 포화 지점에 도달 할 때까지 불포화 용액에서 용매를 증발시킵니다.
- 결정화를 유도하기 위해 과포화 용액에 종자 결정을 첨가하십시오. 결정에 과도한 용질 침전물, 포화 용액을 남겨 둡니다.
- 경우에 따라 불포화 용액의 온도를 낮추면 포화 용액을 형성 할 수있는 용질 용해도가 줄어 듭니다.
포화 용액을 만들지 않는 것
용질과 용매가 포화 용액을 형성 할 수없는 두 가지 상황이 있습니다.
- 불가능한 화학 물질은 포화 또는 기타 용액을 형성하지 않습니다. 예를 들어, 기름과 물이 섞이지 않기 때문에 용액을 만들 수 없습니다. 마찬가지로, 소금과 종이 용액을 만들 수는 없습니다. 화학 물질은 다른쪽에 용해되지 않습니다.
- 마찬가지로, 완전히 잘못된 솔루션은 정의상 모든 비율에 결합하기 때문에 포화 솔루션을 형성하지 않습니다. 예를 들어, 에탄올과 물이 자유롭게 섞여 있습니다. 채도 지점이 없습니다.
기본적으로 불포화, 포화 및 과포화 용액을 형성하려면 용매에 적어도 부분적으로 용해되는 용질이 필요합니다.
참조
- hefter, G.T.; Tomkins, R.P.T (Eds.) (2003). 용해도의 실험적 결정 . Wiley-Blackwell. ISBN 978-0-471-49708-0.
- Hill, J.W.; Petrucci, R. H.; et al. (2004) General Chemistry (4th ed.). 피어슨. ISBN :978-0131402836
- Hülya Demir, Cengiz Özmetin, M.Muhtar Kocakerim, Sinan Yapıcı, Mehmet Çopur. HNO
3 에서 금속 구리 입자의 용해를위한 반 경험적 동역학 모델의 결정 솔루션. 화학 공학 및 처리 :공정 강화 2004, 43 (8), 1095-1100. doi :10.1016/j.cep.2003.11.002 - Petrucci, R.H.; 청어, F.G.; Madura, J.D.; Bissonnette, C. (2010). 일반 화학 :원리 및 현대 응용 (10th ed.). 피어슨 프렌 티스 홀. ISBN :978-0132064521.