많은 학생들이 중학교의 화학 주제에 처음 관여하기 시작할 때 화합물과 혼합물의 개념에 대해 의문을 가질 수 있습니다.
화합물의 정의
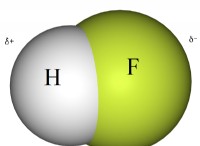
화합물은 둘 이상의 다른 원소로 구성된 순수한 물질이다. 일상 생활에서 염화나트륨과 증류수 (물)는 일반적인 화합물입니다. 화합물은 화합물에 함유 된 각 요소의 상징으로 구성된 화학적 공식에 의해 발현 될 수있다. 예를 들어, 테이블 염 (염화나트륨)의 화학적 공식은 NaCl입니다.
학생들은 원소 물질과 화합물이 원소 관점에서 파생 된 두 가지 개념, 즉 동일한 원소로 구성된 순수한 물질을 원소 물질이라고하며, 다른 원소로 구성된 순수한 물질을 화합물이라고합니다.
화합물과 혼합물의 차이
화학적으로 말하면, 물질은 혼합물과 순수한 물질로 나눌 수 있으며, 순수한 물질은 원소 물질과 화합물로 나눌 수 있습니다. 화합물과 혼합물의 차이는 다음과 같습니다.
1. 화합물의 구성 요소의 특성은 더 이상 원소 상태를 유지하지 않으며, 각 물질은 원래 특성 (예 :고정 용융점 및 비등점)을 유지한다.
2. 화합물의 성분은 화학적 방법으로 분리되어야한다.
3. 화합물의 조성은 일반적으로 일정하다. 혼합물은 특정 조성물없이 혼합 된 다른 물질로 만들어지며 화학적 공식으로 표현할 수 없습니다.
위는 화합물의 정의입니다. 물질이 화합물인지 혼합물인지 여부를 알 수있는 가장 쉬운 것은 화합물이 순수하고 화학적 공식으로 표현 될 수 있지만 혼합물은 그렇지 않으며 화학적 공식이 없다는 것입니다.