질소는 지구 대기의 대부분을 구성합니다 :78.1 % 부피. 그것은 표준 온도와 압력에 너무 불활성이므로 앙투안 라 바오이저의 화학적 명명법 방법에서 "아조 테"( "생명없이")이라고 불립니다. 그럼에도 불구하고 질소는 식품 및 비료 생산의 중요한 부분이며 모든 생물의 DNA의 구성 요소입니다.
특성
질소 가스 (화학 기호 N)는 일반적으로 불활성, 비금속, 무색, 무취 및 맛이 없습니다. 원자 번호는 7이고 원자 무게는 14.0067입니다. 질소의 밀도는 0c에서 1.251 그램/리터이고 비중이 0.96737의 비중을 가지므로 공기보다 약간 가볍습니다. -210.0 ℃ (63k)의 온도와 12.6 킬로 파스 칼의 발발에서 질소는 트리플 포인트에 도달합니다 (요소가 기체, 액체 및 고체 형태로 동시에 존재할 수 있음).
기타 상태
질소의 끓는점 -195.79 C (77k) 미만의 온도에서, 기체 질소는 물과 유사하고 무취 상태로 유지되는 액체 질소로 응축됩니다. 질소는 -210.0 c (63k)의 녹는 점에서 눈이 내리는 푹신한 고체로 굳어집니다.
분자 결합
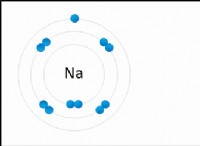
질소는 대부분의 화합물에서 3 막 결합을 형성합니다. 실제로, 분자 질소는 원자의 외부 껍질에있는 5 개의 전자로 인해 가장 강력한 가능한 천연 트리플 결합을 나타낸다. 이 강력한 트리플 결합은 질소의 높은 전기 음성 (Pauling Scale에서 3.04)과 함께 반응성을 설명합니다.
aude
질소 가스는 풍부함과 반응성으로 인해 산업 및 생산 환경에 유용합니다. 식품 생산에서 질소 가스 억제 시스템은 오염에 대한 두려움없이 화재를 소멸시킬 수 있습니다. 산소 또는 수분에 민감한 철, 강철 및 전자 성분은 질소 대기에서 생성됩니다. 질소 가스는 일반적으로 수소 가스와 결합되어 암모니아를 생성합니다.
전위
2001 년, "Nature"는 워싱턴 과학자들의 카네기 기관이 기체 형태를 강렬한 압력으로 삼아 기체 질소를 고체 상태로 변형시킬 수 있다고보고했다. 연구원들은 두 개의 다이아몬드 사이의 질소 샘플을 대기 공기 압력의 170 만 배에 해당하는 힘으로 샘플을 샘플과 비슷한 얼음과 비슷하지만 다이아몬드와 같은 결정 구조로 변형시켰다. -173.15 ° C (100K) 미만의 온도에서 압력이 제거 될 때 샘플은 고체를 유지했습니다. 기체 상태로 되돌아 가면 많은 양의 에너지를 방출 할 때, 리차드 엠 마틴 (Richard M. Martin) 박사는 로켓 연료로 사용한다고 추측 할 수 있습니다.
.