핵심 개념
공명 구조 에 대한이 자습서에서 , 당신은 공명 구조가 무엇인지, 그리고 분자가 가진 가능한 모든 공명 구조를 찾는 방법을 배웁니다. 또한이 구조의 안정성을 식별하고 비교하는 방법을 배웁니다.
다른 기사에서 다루는 주제
- 전기 음성
- 루이스 도트 구조
- 공식 요금
공명 구조는 무엇입니까?
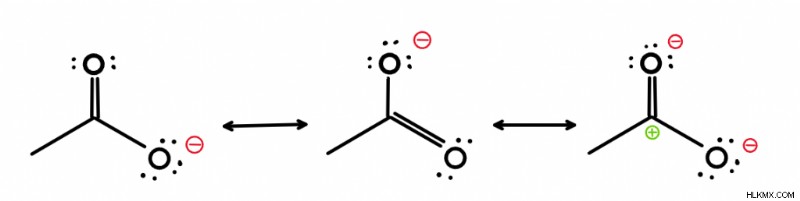
공명 구조는 전자 인 동일한 분자의 다양한 형태입니다. 한 지역에서 다른 지역으로 이송되었습니다.
공명 구조가 중요한 이유는 무엇입니까?
공명 구조는 분자의 모양에 대한 훨씬 더 현실적인 견해를 제공하기 때문에 중요합니다. 각 개별 공명 구조는 공명 하이브리드 로 평균화됩니다. 이것은 분자의 진정한 모양과 가장 안정적인 공명 형태입니다.
분자의 공명 구조를 어떻게 찾습니까?
공명 구조를 그릴 때 명심하고 싶은 몇 가지 사항이 있습니다.
- 전자 만 움직입니다 ( never 원자를 움직입니다).
- 여기에는 고독한 쌍 전자 및 PI 결합이 포함됩니다 (기억 :이중 결합에는 하나의 PI 결합이 있고 트리플 본드에는 2 개의 PI 결합이 있습니다.) .
- 절대 단일 채권 (시그마 본드라고도 함)을 깨뜨립니다.
- 한 번에 한 지역에서 일합니다.
- 이것은 가장 가까운 세 원자에 초점을 맞추고 분자를 내려가는 것을 의미합니다.
- 당신은 전자 밀도 영역에서 시작하고 싶을 것입니다.
- 이것은 전자를 음전하에서 양수로 밀어 올릴 것임을 의미합니다.
- 일반적으로 고독한 쌍을 채권으로 바꾸고 채권을 고독한 쌍으로 바꿀 것입니다.
- 옥켓 규칙을 따르고 큰 공식 혐의를 피하십시오.
예 :오존의 공명 구조를 어떻게 그리겠습니까 (o 3 )?
오존이란 무엇입니까?
먼저 오존을 살펴 보겠습니다. 당신은 아마도 지구의 성층권의 오존층에 대해 들었을 것입니다. "오존층"이라는 이름은 태양의 자외선 방사선의 대부분을 흡수하는 고농도의 오존이 있기 때문입니다. 화학에서는 표준 감소 전위가 큰 대규모 산화제 중 하나입니다.
오존의 루이스 구조
오존의 공명 구조를 찾으려면 오존의 루이스 구조를 그립니다. 분자 공식은 O 3 이기 때문에 , 우리는 18 개의 원자가 전자가 있다는 것을 알고 있습니다 (산소에는 6 개의 원자가 전자가 6 x 3 =18으로). 모든 전자를 배치 한 후, 우리는 이중 결합과 단일 본드를 가질 것입니다.
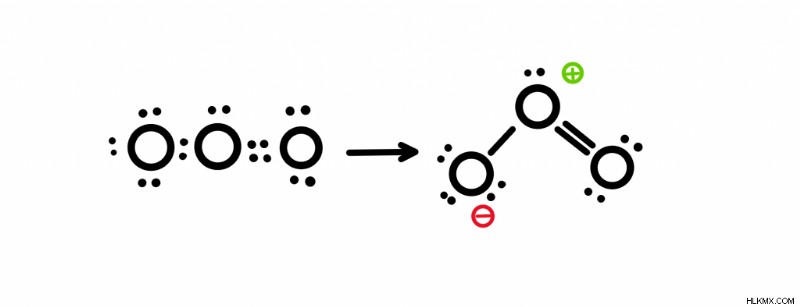
공명 구조 그리기
상단 산소에는 양의 공식 전하가 있고 왼쪽의 산소에 음수가 있습니다. 공식 요금을 찾으려면 원자 가 소유 한 전자 수를 계산하십시오 원자가 전자와 비교하십시오. 예를 들어, 상단 산소는 5 개의 전자를 소유합니다. 전자 2 개는 고독한 쌍이고 다른 3 개는 본드에서 나옵니다. 결합에 전자 중 하나만 소유하고 있습니다. 따라서 6 - 5 =+1. 바닥 산소에 대해서도 마찬가지입니다. 왼쪽 하단에는 7 개의 전자와 6 -7 =-1이 있습니다. 원자가 전자 수를 찾으려면 주기율표 상단의 그룹 번호를 참조하십시오.
1 단계 :음전하로 산소에 전자를 옮기고이를 이중 결합으로 바꿉니다.
2 단계 :양성 산소와 중성 산소 사이의 이중 결합을 깨뜨립니다. 산소에 한 번 단일 결합에 있던 두 전자를 오른쪽에 놓습니다.
3 단계 :이제 오른쪽 하단의 산소에 음전하를 추가하여 공식적인 전하가 -1입니다.
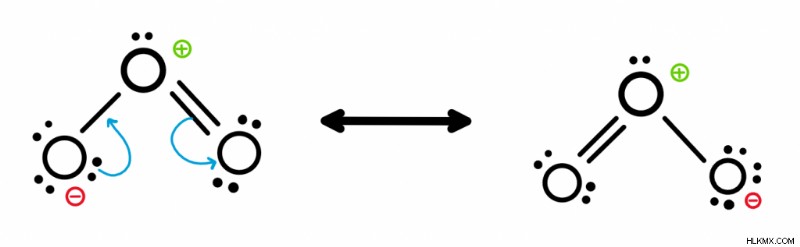
구조물을 분리하는 화살표에 두 개의 헤드가있는 방법에 주목하십시오. 공명 구조는 이것을 사용하여 전자의 흐름을 앞뒤로 보여줍니다. 새로운 독특한 공명 구조를 만들 수 없으면 중지 할 수 있습니다.
가장 안정적인 공명 구조를 어떻게 결정합니까?
에너지가 가장 낮은 공명 구조는 가장 안정적인 것으로 알려져 있습니다. 이것은 단수 구조의 안정성이 클수록 공명 하이브리드에 더 기여하기 때문에 중요합니다. 가장 안정적인 구조는 주요 기여자 로 알려져 있습니다. . 한편, 가장 안정적인 구조는 미성년 기여자 로 알려져 있습니다. . 어떤 공명 구조가 가장 안정적인지 알아 내기 위해 5 가지 주요 규칙이 있습니다. (참고 :두 구조가 같으면 동일하게 기여합니다.)
공명 안정성 규칙 :
- 공명 하이브리드는 단수 구조보다 더 안정적입니다.
- 전하가없는 구조는 충전이있는 구조보다 더 안정적입니다.
- 공식 요금 수가 가장 적은 구조는 더 많은 구조보다 더 안정적입니다
- 가장 안정적인 구조는 음전하 를 갖습니다. 가장 전기 음성 원자 에 배치됩니다 .
- 가장 안정적인 구조는 양전하 를 갖습니다 최소한의 전기 음성 원자에 배치.
예 :가장 안정적인 구조는 무엇입니까?
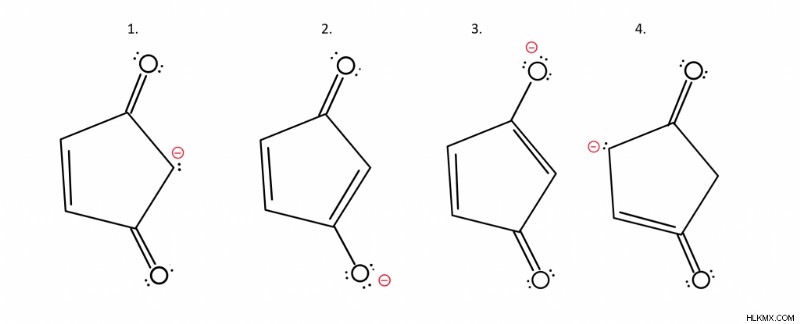
가장 먼저 눈에 띄는 것은 음전하가 각 구조에 대해 다른 영역에 있다는 것입니다. 우리가 알고있는 것으로 되돌아 가면 가장 안정적인 구조는 가장 전기 음성 원자에서 음전하를 갖습니다. 이 경우 산소와 탄소의 두 가지 원자가 있습니다. 어느 것이 더 전기 음성입니까? 당신이 산소를 말하면, 당신은 맞습니다. 따라서 구조 2와 3은 1과 4보다 안정적입니다.
더 안정적이고 구조 2 또는 구조 3?
대답은 그것들이 평등하다는 것입니다. 따라서 주요 기여자와 동등하게 기여할 것입니다.
.추가 읽기 :
채권 주문 대 채권 길이
분자 대 경험적 공식