핵심 개념
이 튜토리얼에서는 위상 다이어그램의 주요 기능 에 대해 배우게됩니다. , 위상 변경 다이어그램 라고도합니다 , 다른 유형의 다이어그램과 그들의 중요성을 해석하고 이해하는 방법.
다른 기사에서 다루는 주제
- 물질 상태
- 압력이란 무엇입니까?
- 고체, 액체, 가스의 특성
- 분자간 힘
- 물리적 대 화학적 특성
- 퓨전 열
어휘
- 응축 - 물질이 기체에서 액체 상태로 갈 때
- 기화 - 물질이 액체에서 기체 상태로 갈 때
- 퓨전 - 물질이 액체에서 고체 상태로 이동하면
- 용융 - 물질이 고체에서 액체 상태로 이동하는 경우
- 승화 - 물질이 고체에서 기체 상태로 직접 이동하는 경우
- 증착 - 물질이 기체에서 고체 상태로 직접 가면
- 위상 변경 - 물질이 한 상태에서 다른 상태로 변할 때 (예 :고체에서 액체 또는 액체에서 가스에서 가스까지)
위상 체이스 다이어그램이란 무엇입니까?
물질이 한 물질 상태에서 다른 상태로 변할 때 위상 전이가 발생합니다. 물질의 세 가지 주요 상태가 있습니다 :액체, 고체 및 가스.
위상 다이어그램은 여러 변수, 대부분 온도 및 압력에 걸친 물질의 다른 단계를 보여주는 플롯입니다. 다이어그램은 이러한 변수를 변화시키는 것이 특정 물질의 문제에 어떤 영향을 미치는지 보여주는 데 도움이 될 수 있습니다.
압력 온도 위상 다이어그램
압력 온도 위상 다이어그램은 가장 일반적이고 기본적인 유형입니다.
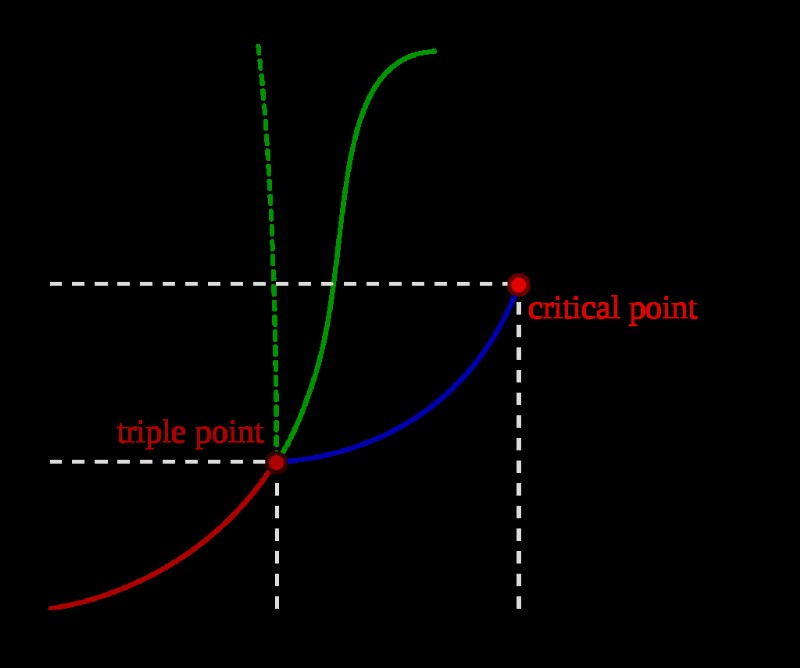
위에 표시된 유형의 위상 다이어그램은 압력 (대기) 대 온도 (섭씨 또는 켈빈도)를 플롯합니다. 실선은 서로 평형에 공존하는 두 단계가 있기 때문에 "공존 곡선"이라고도하는 위상 경계를 나타냅니다. 파란색 선은 비등점 또는 액체와 기체 상태 사이의 전이를 보여주고, 녹색 선은 동결 지점을 나타내거나, 액체와 고형 상태 사이의 전이를 보여주고, 적색 선은 고체 상태가 기체상으로 직접 변환 될 수 있고 그 반대로의 조건을 보여줍니다.
.위상 다이어그램 설명
위상 변경 다이어그램에 대해 배울 때들을 수있는 몇 가지 일반적인 단어와 문구가 있습니다.
융합 (용융 또는 동결) 곡선 - 액체와 고체 상태 사이의 전이를 보여주는 곡선
기화 (또는 응축) 곡선 - 기체와 액체 상태 사이의 전이를 보여주는 곡선
승화 (또는 증착) 곡선 - 기체와 고체 상태 사이의 전이를 보여주는 곡선
트리플 포인트 - 평형에서 가스, 액체 및 고체가 공존하는 온도 및 압력 지점
임계점 - 물질이 액체와 기체 상태 사이에서 구별 할 수없는 온도 및 압력 지점
위상 경계 - 두 물질 상태가 평형에서 공존하는 조건을 나타내는 선
특별한 물의 경우
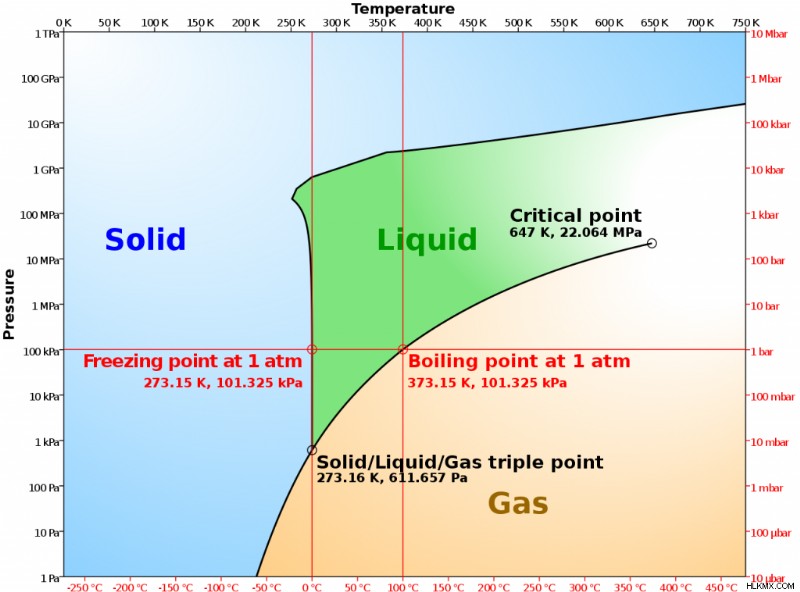
일반적으로 논의되는 특별한 경우는 물의 위상 다이어그램입니다. 위의 다이어그램에서 점선 녹색 선은 물의 위상 다이어그램에서 고체 액체 공존 곡선을 나타냅니다.
.우리는 평균 물질의 경우 액체의 압력을 높이면 곡선을 건너 고체가 될 것임을 알 수 있습니다. 그러나 물의 경우, 고체 (얼음)의 압력을 높이면 곡선을 건너 액체가 될 수 있습니다. 이 거동은 수소 결합으로 인한 많은 양의 여유 공간을 포함하는 얼음의 결정 구조의 밀도가 낮은 결과입니다.
.
다른 유형의 위상 체이스 다이어그램
압력 온도 위상 다이어그램이 유일한 유형은 아닙니다. 부피, 엔트로피, 엔탈피 및 화학 전위를 포함하여 물질의 위상 거동에 영향을 줄 수있는 열역학적 변수가 많이 있습니다. 이러한 변수 중 하나를 사용하여 샘플이 고체, 액체 또는 기체인지를 보여주는 위상 다이어그램을 생성 할 수 있습니다.
2 차원 다이어그램은 두 개의 변수 만 축으로 만 표시 할 수 있으므로,이 변수 가이 변수가 일정 한 위치를 보여주는 곡선으로 세 번째 변수가 표시됩니다. 그것들은 그들이 나타내는 변수에 따라 다른 이름을 가지고 있습니다. 예를 들어, 이소 바는 일정한 압력, 등온수 상수 부피 및 등온선 상수 온도를 나타냅니다.
3D 위상 다이어그램
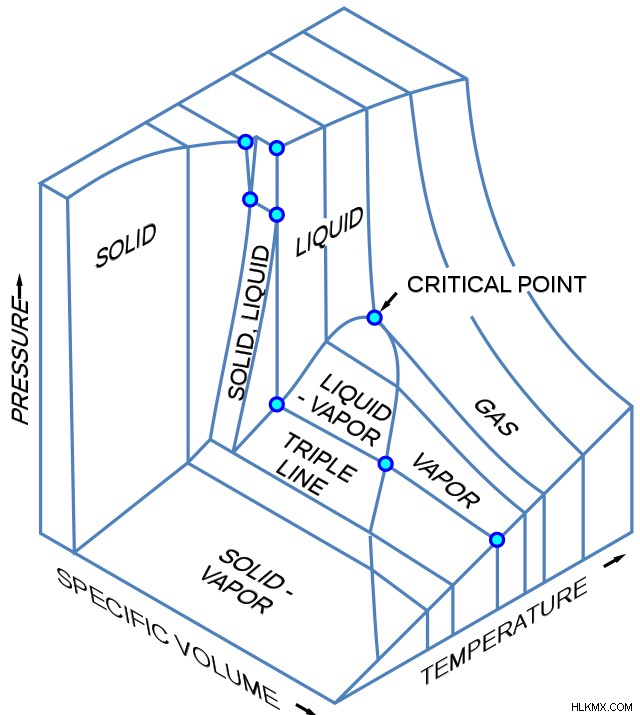
3 차원 위상 변경 다이어그램은 3 개의 열역학적 변수를 플로팅하고 다른 단계에 해당하는 공간 영역을 보여줍니다. 이 유형의 다이어그램에는 트리플 라인 가 있습니다. 트리플 포인트 대신, 공존 표면 공존 곡선 대신. 아래는 일반 3D 다이어그램 플롯 온도, 압력 및 특정 부피입니다.
이진 혼합물
이진 혼합물은 조성에 대한 위상 다이어그램을 가지고 있으며, 일반적으로 하나의 구성 요소의 몰 분율로 표시됩니다. 이것은 혼합물의 위상 거동이 샘플의 특정 구성에 어떻게 의존하는지 보여줍니다. 이 유형의 플롯의 가장 중요한 특성 중 하나는 Eutectic Point 입니다. , 이것은 녹는 점이 가장 낮고 일반적으로 중간 어딘가에 떨어진 다이어그램의 지점입니다. 아래 다이어그램에서는 약 40 mol % 질산염에서 공융 지점을 찾을 수 있습니다.
결정 및 다형성
결정질 고체는 열역학적 변수에 따라 다중 가능한 구조를 가질 수 있습니다. 그렇기 때문에 누군가가 Ice II, Ice III 또는 Ice IV와 같은 다양한 형태의 얼음에 대해 이야기하는 것을들을 수 있습니다. 또한 동일한 물질의 결정 상 (다형성) 인 방해석 및 아라고 나이트와 같은 동일한 화학적 공식을 가진 여러 미네랄을 볼 수 있습니다. 이와 같은 경우, 많은 단계가있는 위상 다이어그램을 보는 것이 일반적이며, 모두 견고합니다.
추가 읽기 - 위상 변경 다이어그램
깔끔한 과학 트릭 :즉시 물을 얼려서 (Susan Koch의 블로그에서)
- 수율
- 일반적인 이온 효과
- 원자가 전자
- 뉴먼 프로젝션
- 공동 특성
- 본드 엔탈피
- Clausius Clapeyron 방정식