핵심 개념
이 튜토리얼에서는 본드 Polar 을 만드는 이유에 대해 논의 할 것입니다. , 어떻게 극성 공유 결합 극성 공유 결합의 예, 그리고 마지막으로 극성 질문을 해결하기위한 단계.
다른 기사에서 다루는 주제
- 화학 결합이란 무엇입니까?
- 전기 음성
- 극성 대 비극성
- 수소 결합
- 이온 다이폴 세력
결합의 극성을 결정하는 것은 무엇입니까?
극성의 특성은 분자 또는 화합물 전체의 전하 분포로 구성됩니다. 분자는 반대쪽 끝에 반대 전하가있을 때 극성입니다. 이러한 전하는 분자의 원자 사이에 전자의 불평등 한 공유에서 비롯됩니다. 반대로, 전자가 분자 전체에서 동일하게 공유 될 때 결합은 비 극성으로 간주됩니다. 극성 분자의 일반적인 예를 조사하여 불평등 한 공유의 예를 살펴 보겠습니다. 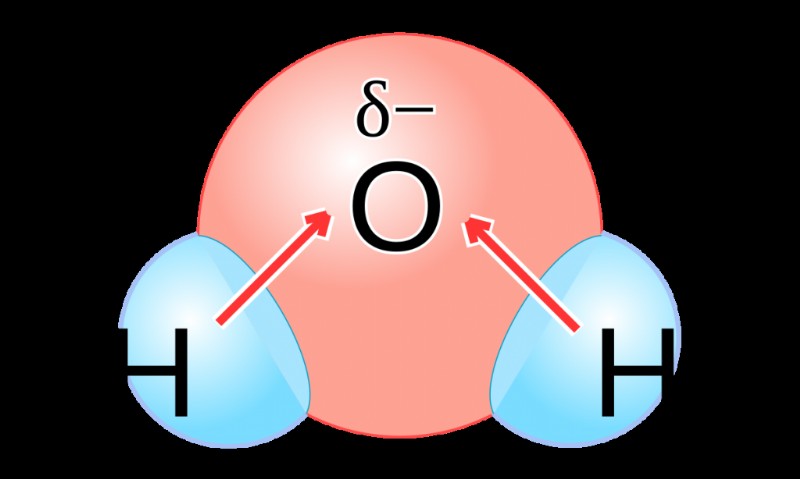
다른 원자는 이미 가지고있는 원자가 전자 수에 기초하여 다른 전기 성분을 갖는다. 전기성이 다른 원자는 전자를 불평등하게 끌어냅니다. 이로 인해 전자의 불평등 한 공유가 발생하여 결합에서 극성을 유발합니다.
극지 본드 란 무엇입니까?
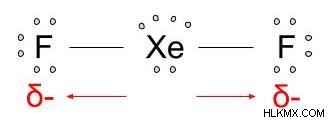
극지 본드가 무엇인지 논의합시다. 극적 결합에서, 두 개의 원자는 전자를 고르지 않게 공유한다. 원자 사이에는 결합이 있으며 전자는 공유되지만 결합의 원자 중 하나를 향해 더 밀접하게 당겨집니다. 전자를 더 밀접하게 당기는 원자는 약간의 음전하를 가지며 다른 원자는 반대 방향으로 약간의 양전하를 갖습니다.
결합은 언제 극성 공유 결합으로 간주됩니까?
극성 공유 결합이란 무엇입니까?
극성 공유 결합은 원자가 공유 결합에서 불평등하게 공유 될 때 발생합니다. 구체적으로, 결합에서 두 원자의 전기성의 차이가 0.4에서 1.7 사이 일 때. 용어 Polar Bond 및 극성 공유 결합 일반적으로 상호 교환 적으로 사용됩니다.
극성 공유 결합 사례
| 본드 | 원자 사이의 전기 음성 차이 | 분자의예 |
| 산소-하이드로겐 | 3.5 - 2.1 =1.4 | 물, H 2 o |
| 카본 클로라이드 | 3.0 - 2.5 =0.5 | 테트라 클로라이드, CCl 4 |
| 질소-하이드로겐 | 3.0 - 2.1 =0.9 | 암모니아, nh 3 |
| 황산소 | 3.5 - 2.5 =1.0 | 이산화황, 그래서 |
| 수소-브로민 | 2.8 - 2.1 =0.7 | 수소 브로마이드, HBR |