핵심 개념
이 튜토리얼에서는 기하학적 이성질체에 대해 모두 배울 수 있습니다 . 이것은 우리가 다른 유형의 이성질체를 정의하고 논의하는 이성질체의 개념에 대한 소개로 시작합니다. 그런 다음 알켄과 사이클로 알칸 모두에서 기하학적 이성질체를 탐색합니다. 그 과정에서 기하학적 이성질체에 대한 시스 트랜스 표기법과 E-Z 표기법의 차이에 대해 배울 것입니다.
다른 기사에서 다루는 주제
- 입체 이성질체 및 키랄 센터
- 입체 방해
- 유기 화학의 기능 그룹
- alkenes
- 의자 형태
- 뉴먼 프로젝션
이성질체는 무엇입니까?
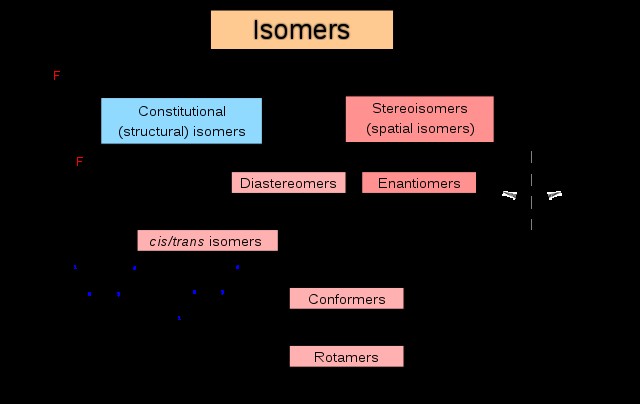
이성질체는 동일한 화학적 공식을 공유하지만 원자의 다른 배열을 갖는 분자이다. 이성질체에는 두 가지 유형의 이성질체가 있습니다 :헌법 이성질체와 입체 이성질체. 헌법 이성질체 (구조 이성질체라고도 함)는 원자가 서로 연결되거나 결합되는 방식이 다르고, 입체 이성질체는 원자의 공간 배열이 다릅니다.
입체 이성질체는 거울상 이성질체와 입체 이성질체의 두 가지 범주로 더 나눌 수 있습니다. 거울상 이성질체 (광학 이성질체라고도 함) 서로. 입체 이성질체 반면에, 미러 이미지가 아닌 입체 이성질체 서로. 또한, 거울상 이성질체는 동일한 화학적 및 물리적 특성 (광학 회전 제외)을 가지고 있지만, 입체 이성질체는 상당히 다른 화학적 및 물리적 특성 (예 :끓는점, 용해도 및 반응성)을 가질 수 있습니다. 시스-트랜스 이성질체 및 입체 형태 이성질체 (즉, 준수제)는 특정 유형의 입체 이성질체이다.
기하학적 이성질체 소개
시스-트랜스 이성질체로도 알려진 기하학적 이성질체는 입체 소성기의 한 형태이다. 모든 입체 이성질체와 마찬가지로, 기하학적 이성질체는 동일한 구성 원자로 구성되고 동일한 시퀀스로 연결되어 있지만 공간에서의 원자의 방향이 다릅니다.
모든 기하학적 이성질체는 분자 내에서 제한된 회전이 필요하여 기능 그룹은 화학적 결합 주위에서 자유롭게 회전 할 수 없게한다. 이 제한된 회전은 일반적으로 탄소-탄소 이중 결합 또는 고리 구조에 의해 발생합니다.
알켄의 기하학적 이성질체
탄소-탄소 이중 결합을 함유하는 화합물에서 기하학적 이성질체에 대한 하나의 주요 요구 사항이있다. 각 이중 결합 탄소 원자는 두 개의 다른 원자 또는 기능 그룹에 부착되어야합니다.
아래에 도시 된 예에서, 첫 번째 쌍의 화합물은 각각의 이중 결합 탄소 원자가 메틸기 및 수소 원자 (즉, 2 개의 다른 그룹)에 부착되기 때문에이 요구 사항을 충족시킨다. 반면에 두 번째 화합물 쌍은 이중 결합 탄소 원자 중 하나가 2 개의 수소 원자 (즉, 두 개의 동일한 그룹)에 부착되기 때문에 요구 사항을 충족시키지 못합니다.
.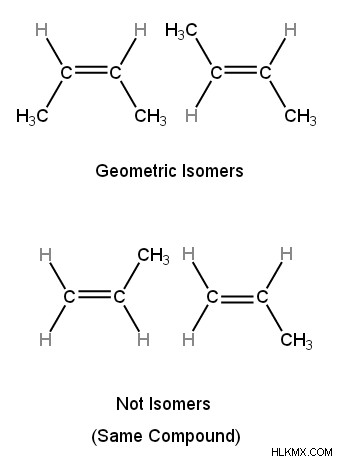 기하학적 이성질체에 대한
기하학적 이성질체에 대한 CIS- 트랜스 표기법
라틴 접두사 cis 및 트랜스 “이쪽에있는”과“반대편의 다른 쪽”으로 번역하십시오. 이들 라인을 따라 CIS 이성질체는 이중 결합의 동일한쪽에 기능 그룹을 갖는 반면, 트랜스 이성질체는 이중 결합의 반대쪽에 작용기를 갖는다.
.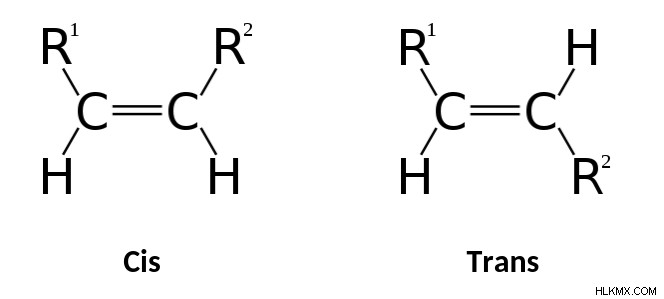 기하 이성질체에 대한
기하 이성질체에 대한 e-Z 표기법
탄소-탄소 이중 결합은 일반적으로 치환기 수 (수소 이외의 원자 또는 그룹)에 따라 분류됩니다. 알켄 치환 패턴의 예는 다음과 같습니다.
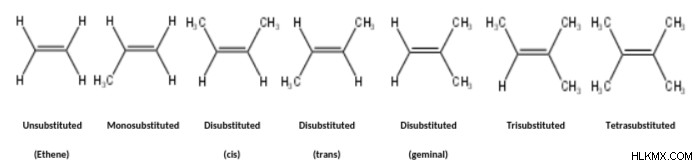
비록 cis 및 트랜스 불가분의 알켄에 대한 기하학적 이성질체를 식별 할 때 유용하며, 3 ~ 4 개의 치환기를 가진 알켄에는 적용되지 않습니다. 반면에 E/Z 시스템은 비정상적인, 삼각형 및 4 트라 비 시스팅 된 알켄에 적용됩니다.
E/Z 이름 지정 시스템을 사용할 때 따라야 할 두 가지 주요 단계가 있습니다.
- 1 단계 :Cahn-ingold-Prelog 규칙을 사용하여 이중 채권의 양쪽에서 더 높은 우선 순위 그룹을 식별하십시오. 이 규칙은 여기에 자세히 설명되어 있습니다.
- 2 단계 :두 개의 높은 우선 순위 그룹이 탄소 탄소 이중 결합의 동일 또는 반대쪽에 있는지 여부를 결정하고 e 를 할당합니다. 또는 z 따라서.
구성 z를 갖는 이성질체 (독일어 Zusammen ,“함께”를 의미) 이중 결합의 동일한 측면에서 우선 순위가 높은 치환기를 갖는 반면, 구성 E (독일어 Word entgegen 의 이성질체 ,“반대”를 의미) 이중 결합의 반대쪽에 우선 순위가 높은 치환기가 있습니다.
E/z 명명 시스템을 사용한 기하학적 이성질체의 두 가지 예가 다음과 같습니다. 위에서 설명한 단계에 따라, 각 이성질체는 e 에 제공됩니다. 또는 z 지정.
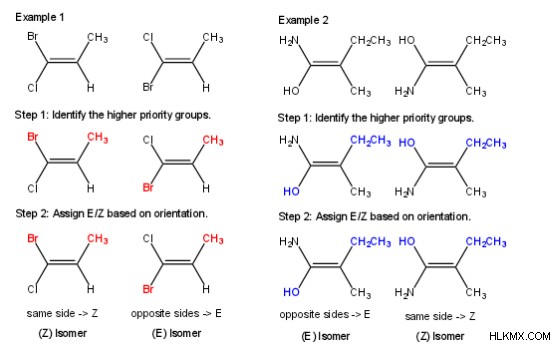 사이클로 알칸의
사이클로 알칸의 기하학적 이성질체
주기적 화합물을 다룰 때 쐐기와 대시는 링의 치환기의 상대적 배향을 나타내는 데 사용됩니다. 쐐기는 링 평면 위의 화학적 결합을 나타내며 (즉, 당신을 향해 오는) 점선은 링 평면 아래의 화학적 결합을 나타냅니다 (즉, 당신에게서 멀어짐).
.기하학적 이성질체는 일반적으로 불분명 한 사이클로 알칸에서 관찰됩니다. 시스 이성질체는 동일한 방향을 갖는 2 개의 치환기를 갖는다 (2 개의 웨지 또는 2 개의 점선으로 표시됨). 한편, 트랜스 이성질체는 반대 방향을 갖는 2 개의 치환기 (하나의 쐐기와 하나의 점선으로 표시)를 갖는다.
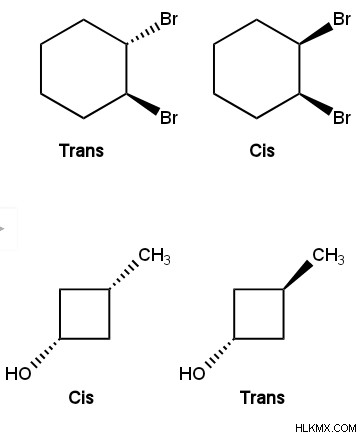
사이클로 알칸은 E-Z 표기법을 사용하지 않으므로 탄소 탄소 이중 결합이 필요합니다.
또한 두 기능적 그룹이 동일한 탄소에 부착 될 때 기하학적 이성질체는 비 혼란에 적용되지 않는 시클로 알칸에 적용되지 않는다는 점에 주목하는 것이 중요하다. 예를 들어, 1- 플루오로 -1- 메틸 시클로 헥산 (아래 그림)은 기하 이성질체가 없으며 시스 또는 트랜스 지정이 제공되지 않습니다.
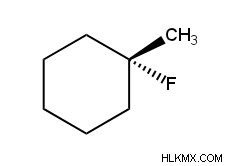
추가 읽기
- 공명 구조
- 탄수화물 안정성
- SN1 대 SN2 반응
- E1 대 E2 반응 이해