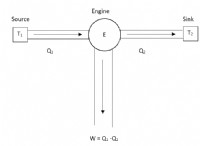
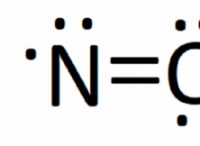전자 성 치환 반응은 electrophile이 물질의 기능 그룹을 변화시키는 화학 절차입니다. 일반적으로 실용적인 변위 그룹은 수소 원자입니다. 전자 성 치환 반응은 일반적으로 3 단계로 수행됩니다.
유기 물질에 의해 발생하는 두 가지 주요 종류의 전자 성 치환 반응은 향기로운 전자 성 대체 및 전자 성분 대체 반응입니다.
전자 성 방향족 치환 반응
전기성 치환 반응은 유기 절차에서 전기성이 고리에 연결된 원자를 대체하거나 대체 할 때 발생합니다. 이것은 확실히 방향족이며, 전기성을 갖는 벤젠 밴드로부터의 수소 원자의 치환은 이러한 반응에서 일반적이다.
.이 향기로운 시스템의 방향족은 전자 성 방향족 대체 효과 내에서 유지됩니다. 고리의 안정성은 의심 할 여지없이 방향족이며, 아마도 브로 모 벤젠이 벤젠과 브롬의 반응으로 인해 생성 될 때마다 영향을받지 않을 것입니다. 이 반응에 따라 다이어그램이 의심 할 여지없이
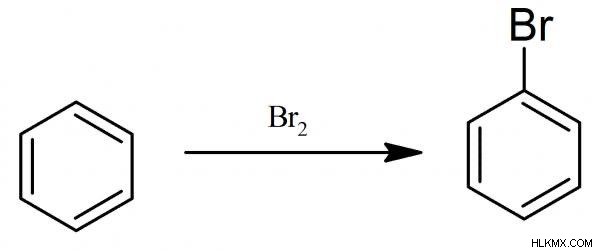
전기성 치환 반응은 전기성이 물질에 사용 된 결합 된 그룹을 대체 할 때입니다. 전자 유형의 예는 H3O+, HCl, HBR, HI, NO2+및 SO3입니다.
재배치 된 기능 그룹은 주로 H입니다.
교체품에서 의심 할 여지없이 전자성. 전기성의 치환은 많은 방향족 반응 (함유 된 화합물 벤젠)에서 발견되며, 이는 방향족 인 전자 유전 적 대체로 악명 높은 것으로 알려져있다. 전자 성 치환은 지방족이다.
이 반응과 관련된 세 단계는 다음과 같습니다.
-
전기를 가져 오는 것.
-
다음 단계는
사이에 작용할 탄수화의 개발입니다. -
마지막 단계는 양성자를 제거하는 것입니다.
벤젠의 기본 유형의 벤젠 대체 반응은 다음과 같습니다. -
-
알킬화
-
아실화
-
할로겐화
-
질산
-
설 폰화 등
elecropholic substitution 반응은 일반적으로 세 가지 수준으로 똑바로 고정됩니다.
• electrophile의 출현
• 탄수화물 형성 (중간이 될 수 있음)
• 중간체에서 양성자 추출
전자 성 치환 반응의 유형
-
전자성 방향족 치환 효과
향기로운 고리에 장착 된 원자는 전자 성 방향족 대체 반응에서 전기성을 갖는 것에 의해 변경됩니다. 이러한 반응에는 방향족 질화, 방향족 설 폰 화 및 프리델크 레크래스 반응이 포함됩니다.
요소에 대한 방향족은 전자적 향미 대체에서 확실히 방향으로 보존된다는 것을 기억하는 것이 중요합니다. 전자 성 할로겐화는 요오드, 염소 또는 브롬을 갖는 방향족 또는 향기로운 고리 인 아릴 할라이드 또는 할로 레네를 생성 할 수 있습니다. 알루미늄 트리 할라이드는 일반적으로 이러한 과정에서 촉매로 사용됩니다.
-
전자성 지방족 치환 반응
전자 성 치환 반응에서 기능 그룹은 지방족 화학 물질 내의 전기로 대체됩니다. 이 응답은 다섯 가지 종류로 분류됩니다 :
-
케톤의 할로겐화
-
공증
-
케토 에놀 타우티머
-
카르 벤을 탄소 하이드로겐 관계에 바로 삽입
-
디아 조 늄 커플 링 (지방족)
할로겐화
할로겐화 :항목 또는 화합물에 하나 이상의 할로겐을 포함시키는 반응입니다. 할로겐과 화학량 론의 메커니즘은 천연 기질의 건축 적 특성과 귀중한 범주와 할로겐에 의존합니다. 무기 화합물은 또한 할로겐화를 거치지 만 금속은 그렇지 않습니다.
할로겐화 유형
두 가지 형태의 할로겐화가 있습니다. 예는 에텐에 브롬을 첨가하는 것일 수있다. 할로겐은 열 또는 빛에 의해 술에 취한 알칸과 반응하여 알킬 할라이드를 형성한다. 할로겐 원자로 인해 알칸으로의 수소가 바뀌 었습니다. 이는 이것이 대체 반응임을 의미합니다.
할로겐화 방향족 화합물
향기로운 화합물의 할로겐화는 할로겐화 반응입니다. 이것은 의심 할 여지없이 전자적입니다.
rc6h5+ x2hx+ rc6h4x
이 할로겐화 과정은 할로겐 요소의 영향을받습니다. 불소와 염소는 전자 성 특성을 가지므로 더 강력한 할로겐화 대표자를 초래하고 브롬은 약한 중개인입니다. 이것은 확실히 불소와 염소에 할로겐화이지만 요오드는 이것에 가장 약한 것일 수 있습니다. 이 탈 하이드로 할로겐화의 메커니즘은 역전 경향을 사용합니다. 요오드는 자연 물질을 제거하기가 가장 쉬울 수 있으며 유기 불소는 확실히 가장 높은 안정성을 가지고 있습니다.
.결론
방향족 인 전자 유전 적 치환은 주로 염소와 브롬과 같은 할로겐이 필요합니다. 이 반응은 또한 Halogen-Halogen 관계를 분극하는 데 주로 사용되는 Fe3+ (실험실 방법)와 같은 Lewis 산을 볼 때도 수행됩니다. 전자 성 치환 반응은 전기성이 물질의 기능 그룹을 변화시키는 화학적 절차입니다. 할로겐화는 항목 또는 화합물에 하나 이상의 할로겐을 포함시키는 물질 반응입니다.