그것은 비대칭적이고 대칭적인 에테르를 준비하는 데 중요한 방법 인 Williamson 합성으로 시작합니다. 에테르는 2 개의 알킬기 사이에 산소를 함유하는 유기 화합물이다. 이는 R이 알킬 그룹이고 O는 산소입니다. 에테르는 알콕시 알칸으로도 알려져 있습니다. 그들은 향수, 오일, 왁스 및 염료에 널리 사용됩니다. 이 반응에서, 알킬 할라이드는 알코폭 사이드 나트륨과 반응한다. 대체 알킬기를 가진 에테르는이 방법으로도 만들 수 있습니다.
에테르를 만드는 알코올의 탈수
알코올을 탈수하여 에테르를 성공적으로 만들려면 올바른 온도를 갖는 것이 필수적입니다. 알코올 컨쥬 게이트 산의 SN2 반응은 110 ° 내지 130 ℃에서 에테르를 생성하고, Adobe 150 ℃의 온도에서, E2 제거가 발생한다.

위의 반응에서 온도는 약 413k로 유지되고 알코올은 초과됩니다. 이 두 절차의 반응이 정확하게 따르지 않으면 알코올은 탈수를 겪고 알켄을 생성합니다. 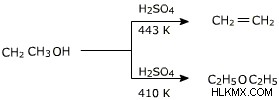
주요 생성물은 에탄올이 433k의 온도에서 황산의 존재하에 에테르로 탈수 될 때에 톡시 에탄이 될 것이다. 이 반응에서 알켄이 빠르게 형성되기 때문에 2 차 및 3 차 알코올의 탈수에 의해 에테르를 얻는 것은 불가능합니다. 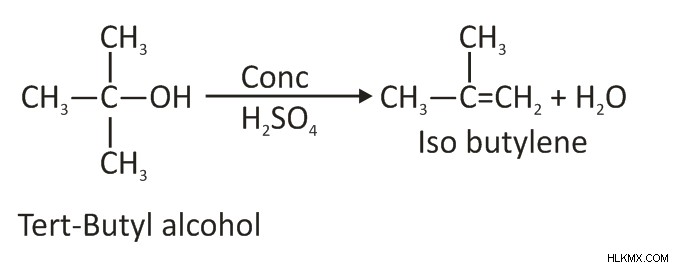
상기 주사 반응은 생성물의 혼합물을 얻어야하기 때문에 비대칭 에테르를 생성하는 데 사용될 수 없습니다. Alkoxymercuration을 사용하여 비대칭 에테르를 생성 할 수 있습니다.
상기 주사 반응은 생성물의 혼합물을 얻어야하기 때문에 비대칭 에테르를 생성하는 데 사용될 수 없습니다. Alkoxymercuration을 사용하여 비대칭 에테르를 만들 수 있습니다.
에테르의 명칭
-
에테르의 공통 이름은 에테르 산소에 연결된 두 그룹을 참조하여 제공 될 수 있습니다. 예를 들어,

-
알킬 알칸, 알 콕시 알칸 및 알킬 렌과 같은 IUPAC 이름. 이것에서 가장 긴 체인은 루트 단어와 부모 체인입니다.
에테르의 화학적 특성
에테르는 과일 냄새를 가진 무색이거나 투명한 유체이며 가연성이 높습니다. 에테르는 또한 H- 결합 및 소수성 알킬기 때문에 물에 용해된다. 그럼에도 불구하고, 그들은 수소 결합이 부족하므로 에테르의 끓는점은 다른 알코올보다 훨씬 적습니다. 디 에틸 에테르는 또한 마취제로 사용될 수있다. 에테르의 결합 각도가 약 110 °의 결합 각도를 가지므로 C-O 결합의 움직임은 취소되지 않으므로 극성이 매우 약합니다.
에테르의 물리적 특성
물 분자와의 에테르의 수소 결합 형성은 물에 최대 3 개의 탄소 원자를 함유 할 수 있기 때문에 용해도는 감소하여 탄화수소 원자의 증가가 H- 결합의 형성을 감소시킨다. 그들은 공식 R-O-R을 가지고 있으며 알킬기 사이에 SP3 하이브리드 산소를 함유합니다. 아릴 에테르에서 산소의 고독한 쌍 전자는 에테르의 특성을 변화시키는 방향족 고리와 2 개의 화합물의 결합에 의해 형성된다.
에테르에서 C-O 결합의 절단
에테르에서 C-O 결합의 절단은 초과 HX 및 고온으로 극한 조건 또는 변화가 필요합니다. Dialkyl Ether와 HX의 반응은 알킬 할라이드의 두 분자를 제공합니다.
r-o-r+hx → r-x+r-oh
알킬 아릴 에테르는 더 안정적인 아릴 산소 결합으로 인해 알킬 산소 결합에서 절단되며,이 결합을 파괴하는 것은 어렵다. 반응성의 순서는 HI> HBR> HCL입니다. 반응 조건 :초과 (conc.) HI 또는 HBR 및 고온.
우리가 에테르가있을 때, 두 개의 다른 알킬기도 비슷하게 절단됩니다.
r-o-r '+hx → r-x+r'-oh
여기서 메커니즘은 첫 번째 단계가 에테르의 양성자화라는 것입니다. 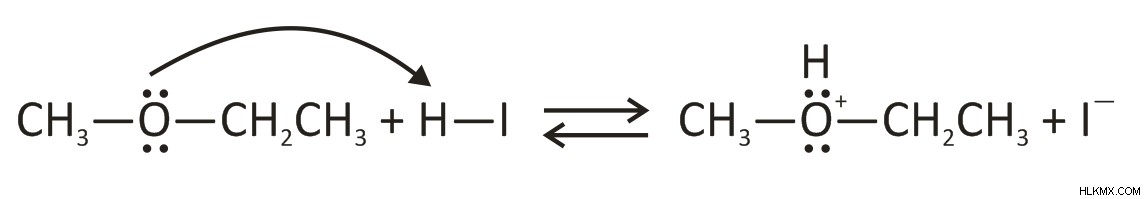
에테르는 산성 매체에서 양성자 화 된 다음 에테르로 양성자가 있습니다.
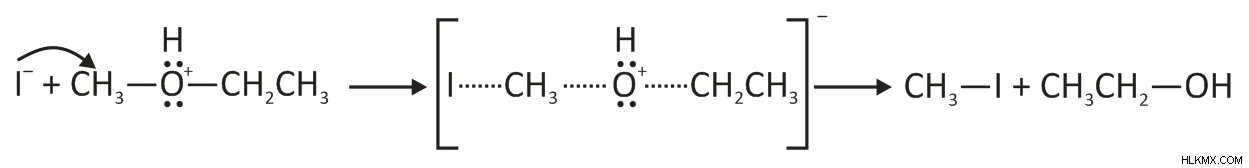
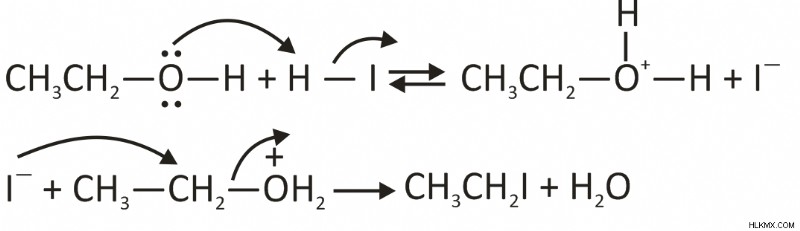
그러면 두 번째 단계는 SN2 반응이 발생하는 곳입니다. 우리는 I- 메틸 그룹을 유치 한 다음 살아있는 그룹이 알코올 및 메틸 요오드화물 인 전이 상태가 있음을 알 수 있습니다. 우리는 과량의 HI 및 고온을 가지므로, 또 다른 치환 반응이 우리에게 알킬 요오드화의 다른 분자를 제공합니다.
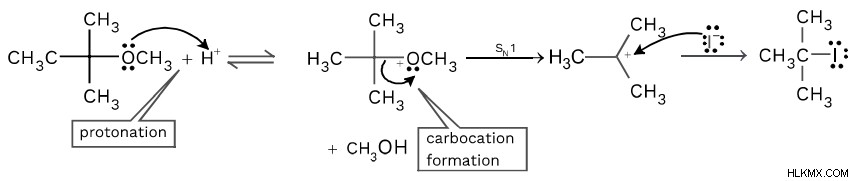
이 경우 알킬 그룹 중 하나가 3 차 일 때 어떤 일이 발생하는지 볼 수 있습니다. Halide 결과는 또한 3 차 할라이드입니다.

두 번째 단계에서, SN1 메커니즘은 탄수화물이 형성되는 곳에서 발생합니다.
결론
우리는 비대칭 및 대칭 에테르에 대해 논의했습니다. 우리는 에테르가 2 개의 알킬 그룹 사이에 산소를 함유하는 유기 화합물이며 알코올의 탈수에 의해 에테르를 만드는 방법에 대해 논의했다. 공정 중에 올바른 온도를 갖는 것이 중요합니다. C-O 결합의 절단은 반응 시간, 용매 및 온도와 관련이있다. 높은 수소 가스압 및 유기 용매가없는 경우, 촉매는 용매로서 물에서 C-O 결합의 절단을 효율적으로 촉매 할 수있다. 카르 보닐 산소의 양성자 화는 알코올의 친 핵성 첨가를 향해 카르 보닐기를 활성화시킨다.