화학적 결합은 자연의 힘이며 원자, 이온 등과 같은 다양한 화학 성분을 함께 결합합니다. 화학적 결합은 에너지 방출로 안정성을 얻기 위해 형성됩니다.
하이브리드 화는 원자 궤도를 혼합하여 전자의 쌍이 적합한 원자 궤도를 갖는 새로운 하이브리드 궤도를 형성하는 과정이다.
본드 각도
결합 각은 두 개의 인접한 결합 사이의 기하학적 각도입니다. 결합 각도는 결합 전자를 함유하는 궤도를 나타내는 선 사이의 각도로 정의됩니다. 모양을 결정하는 데 도움이되고 정도로 표현 될 수 있습니다.
하이브리드 화
하이브리드 화는 에너지를 재분배하기 위해 약간 다른 에너지를 갖는 궤도를 혼합하는 과정입니다.
혼성화의 특징
(i) 거의 동일한 에너지를 가진 궤도는 혼성화에 참여합니다.
(ii) 원자 궤도의 수는 생성 된 하이브리드 궤도의 수와 같습니다.
(iii) 하이브리드 화는 공유 분자의 형상을 나타낼 수 있습니다.
(iv) 하이브리드 궤도는 순수한 원자 궤도보다 더 효과적인 결합을 형성 할 수 있습니다.
혼성화에 필요한 조건 :
(i) 원자가 껍질의 궤도는 혼성화에 참여합니다.
(ii) 혼성화에 관여하는 궤도는 거의 동일한 에너지를 가져야합니다.
(iii) 혼성화에서 전자의 촉진은 필요한 조건이 아닙니다.
(iv) 경우에 따라, 가득 채운 궤도의 궤도도 혼성화에 참여합니다.
원자가 쉘 전자 쌍 반발 (VSEPR) 이론
이 이론은 다음과 같습니다.
1. 중앙 원자의 원자가 쉘에서 발견되는 전자 쌍의 수는 다양한 분자와 이온의 형상을 결정합니다.
2. 전자 쌍은 최소 반발 상태를 얻기 위해 가능한 한 멀리 머무르려고 노력합니다.
3. 결합 된 전자 쌍의 유사한 원자가 중앙 원자를 둘러싸고 있으면 반발 상호 작용이 동일하고 분자 기하학이 규칙적입니다.
4. 비 유사한 원자의 결합 된 전자 쌍이 중심 원자를 둘러싸고있는 경우, 반발 상호 작용은 동일하지 않습니다. 따라서 분자의 형상은 규칙적이지 않습니다.
5. 전자의 결합 쌍 (BP) 및 고독한 쌍 (LP)이 중심 원자를 둘러싸고있는 경우, 반발 상호 작용은 동일하지 않습니다. 따라서 분자의 기하학은 불규칙합니다.
반발 상호 작용은 순서 :
고독한 쌍 결합 쌍 트리 플루오 라이드의 분자 형상 및 결합 각도에 대해 배우려면 혼성화에 대해 논의해야합니다. 염소 트리 플루오 라이드의 혼성화에 대해 이야기 할 때, 우리는 그 중심 원자, 염소를 고려해야합니다. 중앙 원자는 7 개의 원자가 전자를 함유하고 Clf3은 3 개의 결합 쌍과 2 개의 고독한 쌍으로 구성됩니다. CL의 원자가 쉘 전자 구성은 3S2, 3PX2, 3PY2, 3PZ1, 3D로 제공됩니다. 염소가 불소 원자와 결합하여 CLF3을 형성 할 때, 3 개의 F- 원자와 결합을 생성하려면 3 개의 짝을 이루지 않은 전자가 필요합니다. 3p 서브 쉘에서 CL의 한 쌍의 전자는 고독한 쌍으로 남아 있거나 짝을 이루지 않은 채로 남아 있습니다. 결과적으로, 하이브리드 화 중에, 1 개의 3, 3 개의 3p 및 3D 궤도 중 하나 가이 과정에 참여하여 5 개의 SP3D 하이브리드 궤도가 형성됩니다. 이제 2 개의 하이브리드 궤도에는 한 쌍의 전자가 포함되며 3 개의 하이브리드에는 짝을 이루지 않은 전자가 있으며, 이는 단일 결합을 형성하기 위해 F의 2p 궤도와 겹치게됩니다. 염소의 중앙 원자는 3 개의 f- 아톰과 결합하기 위해 3 개의 짝을 이루지 않은 전자를 필요로합니다. clf3는 이제 3 개의 본드 쌍과 2 개의 고독한 쌍으로 구성됩니다. 1 개의 3, 3 개의 3p 및 3D 궤도 중 하나가 하이브리드 화에 참여하면 5 개의 SP3D 하이브리드 궤도가 형성됩니다. 분자 형상은 분자에서 원자의 3 차원 구조 또는 배열이다. 트리 플루오 라이드의 분자 형상과 결합 각도에 대해 논의 해 봅시다. 염소 트리 플루오 라이드의 구조는 3 개의 불소 원자로 둘러싸인 1 개의 염소 원자로 구성됩니다. 그 구조에는 중앙 염소 원자에 부착 된 2 개의 고독한 전자 쌍이 있습니다. 염소 원자는 안정적인 상태에서 주변 불소 원자와 3 개의 공유 결합을 형성합니다. 중심 염소 원자의 혼성화는 SP3D입니다. CLF3의 분자 형상은 T 자형이라고합니다. CLF3은 두 개의 고독한 쌍이 더 많은 공간과 더 큰 반발이 필요하므로 적도 위치를 차지하기 때문에 이러한 모양을 얻습니다. 그것들은 3 개의 결합과 2 개의 고독한 쌍을 가진 삼각형 bipyramidal 모양으로 배열됩니다. 중앙 원자 주변에서 발견되는 비대칭 전하 분포도 있습니다. 염소 트리 플루오 라이드의 분자 형상 및 결합 각은 175 ° F-C-F 결합 각도를 가진 삼각형 이피 라달입니다. 화학적 결합은 서로 다른 원자의 전자가 상호 작용하여 이들 원자가 분리 될 때보 다 더 안정적인 배열을 생성 할 때 형성됩니다.
CLF3의 분자 형상 및 결합 각은 1.598Å의 짧은 결합 및 1.698 Å의 2 개의 긴 결합과 함께 175 °의 T 자형이며, 175 °의 F-Cl-F 결합 각도. 이 구조는 VSEPR 이론의 예측을 검증합니다. 이론은 전자의 고독한 쌍이 가상의 삼각형 바이 파리 마이드의 두 적도 위치를 차지한다고 말합니다. 염소 트리 플루오 라이드의 혼성화
분자 형상
분자 구조로도 알려진 CLF3 분자 형상 및 결합 각도
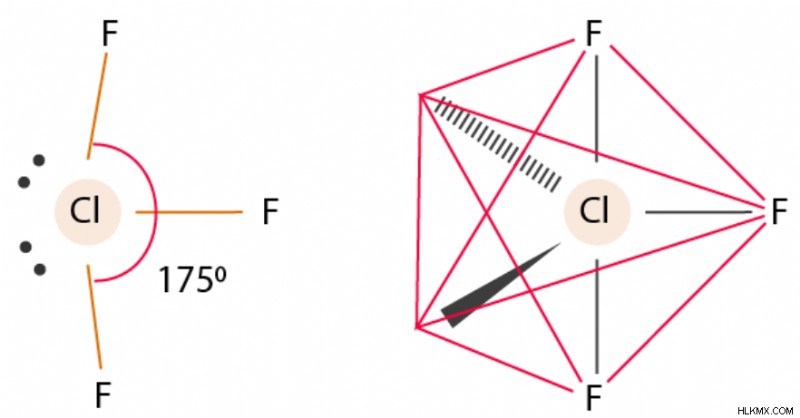
결론