배위 복합체는 코어 원자 또는 이온으로 구성되며, 이온은 일반적으로 금속성이며 조정 센터 및 리간드 또는 복합체로 지칭되는 부착 된 분자 또는 이온의 배열로 구성된다. 배위 복합체는 많은 금속 함유 화합물, 특히 전이 금속을 포함하는 화합물에서 발견된다. [Cu (NH3) 4]는 두 가지 예입니다. Ni (CO) 4; SO4.
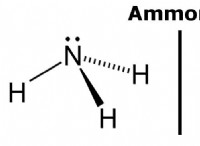
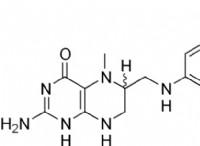
배위 화합물은 비타민 B12, 헤모글로빈 및 엽록소뿐만 아니라 유기 분자의 합성에 사용되는 염료, 안료 및 촉매를 포함한다.
.살아있는 유기체는 자연적으로 발생하는 배위 분자가 필요합니다. 생물학적 시스템에서 금속 복합체는 다양한 중요한 역할을합니다. 금속 복합체 (메탈로 엔자임)는 생물학적 과정을 조절하는 자연적으로 발생하는 촉매 인 많은 효소에서 발견된다. 예를 들어, 소화 불량에 중요한 가수 분해 효소 인 카르복시 펩 티다 제는 단백질의 다중 아미노산 잔기에 조정 된 아연 이온을 갖는다. 철-포르피린 복합체를 포함하는 또 다른 효소는 카탈라아제이며, 이는 과산화수소의 분해를위한 우수한 촉매이다. 헤모글로빈은 또한 철-포르피린 복합체를 함유하고, 산소 수송 체로서의 기능은 산소 분자를 가역적으로 조정하는 철 원자의 능력에 의존한다.
.광 흡수에 의해 트리거 된 전자 전이는 전이 금속 복합체에서 아름다운 색조를 제공합니다. 결과적으로 그들은 자주 안료로 사용됩니다. D –D 전이 또는 전하 이동 대역은 컬러 금속 복합체와 관련된 가장 일반적인 전이입니다. D – D 전이는 부분적으로 채워진 D- 궤도 복합체 (D1-9)에 대해서만 발생합니다 (D1–9)는 금속의 D 궤도의 전자가 광자에 의해 더 높은 에너지의 다른 D 궤도로 자극되기 때문입니다. 그럼에도 불구하고 D -D 전환이 아닌 경우에도 D0 또는 D10 구성을 갖는 복합체에서는 전하 전송이 상상할 수 있습니다. 전자는 금속 기반 궤도로부터 충전 전달 대역 (금속-리간드 전하 전달 또는 MLCT)에서 빈 리간드 기반 궤도로 촉진된다. 빈 금속 기반 궤도 내로 리간드 기반 궤도에서 전자의 여기는 또한 발생합니다 (리간드-금속 전하 이동 또는 LMCT)
조정 복합체의 특성
조정 화합물의 일반적인 특성은이 하위 섹션에서 논의됩니다.
- 전이 요소에 의해 생성 된 배위 화합물에 짝을 이루지 않은 전자의 존재는 전자 전이 동안 빛의 흡수의 결과로 배위 화합물을 채색하게한다. 철 (II) 복합체와 같은 철 (III)을 포함한 배위 화합물의 예는 녹색 또는 옅은 녹색 인 반면, 철 (II)을 함유하는 배위 화합물은 갈색 또는 황갈색입니다.
- 조정 센터가 금속 인 경우, 관련 조정 복합체는 조정 센터에 짝을 이루지 않은 전자의 존재로 인해 자기를 나타냅니다.
- 조정 화합물은 광범위한 화학적 반응성을 나타낼 수있다. 내부 스피어 전자 전달 반응 및 외부 스피어 전자 전달 반응 모두에서, 이들은 부산물로 찾을 수 있습니다.
- 리간드에 따라 복잡한 분자가 분자의 변형에서 촉매 또는 화학량 론적 촉매로서 작용할 수있다.
복합체는 다양한 가능한 반응성을 보여줍니다 :
전자 전송
내부 및 외부 구체 전자 전송은 금속 이온 사이의 전자 전송을위한 두 가지 다른 공정이다. 브리징 리간드는 내부 구체 반응에서 ET의 채널 역할을합니다.
(퇴화) 리간드 교환
퇴화 리간드 교환 속도는 반응성의 주요 척도이다. 불안정한 복합체는 리간드가 방출되어 빠르게 회복되는 복합체입니다. 열역학적으로, 이러한 불안정한 화합물은 상당히 안정적 일 수 있습니다. 불안정한 금속 복합체는 전형적으로 리간드 (Zn2+)에 대한 D- 궤도의 저하 (Na+), 항비 전자 또는 공유가 없음 (LN이 LN이 란타나이드 인 경우)을 함유한다. 스핀 대 저 스핀 구성을 이용할 수있게되면 금속 복합체의 윤활성도 마찬가지로 영향을받습니다. 결과적으로, 높은 스핀 Fe (II) 및 Co (III)는 불안정한 복합체를 형성하는 반면, 낮은 스핀 당량은 비활성이다. 공식적인 산화 상태가 높기 때문에, M – L 안티본 궤도에 전자가없고, D3 구성과 관련된 일부 "리간드 필드 안정화", Cr (iii)는 불활성 인 저-스핀 상태 (사중)에만 존재할 수 있습니다.
.연관 과정
복합체에서 채워지지 않거나 반으로 채워진 궤도는 종종 기질과 반응하는 성향을 나타낸다. 대부분의 기판은 단일지면 상태 또는 고독한 전자 쌍 (예 :물, 아민 및 에테르)을 포함하기 때문에 금속 중심과 반응하려면 빈 궤도가 필요합니다. 일부 기질 (예 :분자 산소)은 삼중 항 접지 상태를 가지며, 이는 반으로 채워진 궤도가있는 금속이 이들과 반응하게 만듭니다 (이산 소 분자는 또한 고독한 쌍을 가지므로 '일반'루이스베이스로 반응 할 수 있음). 금속은 주위의 리간드를 신중하게 선택하면 분자 변형을 돕거나 센서로 사용될 수 있습니다.
조정 화합물의 적용
야금에서,
(a) Dicyanoargentate 및 Dicyanoaurate와 같은 시안화물 복합체의 생산은은 및 금과 같은 고귀한 금속을 광석에서 회수 할 수있게한다.
(b) 금속 조정 복합체의 형성 및 후속 붕괴는 금속을 정화하는 데 사용될 수있다.
니켈은 일산화탄소와 반응하여 정제 될 수 있으며, 순수한 니켈을 생성하기 위해 열적으로 파괴 될 수있는 휘발성 화합물 인 테트라 카르 보닐 니켈 (0)을 생성 할 수있다.
. 생물학적 시스템에서(a) 산소 캐리어 역할을하는 혈액의 적색 안료 인 헤모글로빈은 철분 조정 복합체입니다.
(b) 금속 복합체는 생물학적 과정을 지배하는 다수의 효소에서 발견됩니다.
Carboxypeptidase는 단백질을 가수 분해하고 많은 아미노산 잔기에 공유 결합 된 아연 이온을 함유하는 프로테아제 효소입니다.
. 산업 공정에서(a) 테트라 클로라이드 티타늄 및 트리 에틸 알루미늄의 혼합물 인 Ziegler-Natta 촉매는 Ethene의 중합에 사용됩니다.
(b) 복잡한 금속 촉매는 알켄의 수소화에 사용됩니다.
분석 화학 분야에서
(a) 질적 조사 방법을 사용하여 대부분의 무기 이온의 식별 및 분리에 복잡한 형성이 중요합니다.
(구리 황산염 용액이 수성 암모니아와 결합 될 때 물에 깊은 푸른 복합체가 생성됩니다.)이 과정을 사용하여 소금의 핵 이온이 감지됩니다.
.(b) EDTA의 나트륨 염을 이용한 적정은 물의 경도를 결정하는데 사용된다; 경수의 칼슘 및 마그네슘 이온은 마그네슘 EDTA 및 칼슘 EDTA라고하는 안정적인 복합체를 형성합니다. 마그네슘 및 칼슘 EDTA 복합체의 안정성 상수가 다르기 때문에 이러한 이온은 선택적으로 계산 될 수 있습니다.
결론
FECL4- 이온 및 CRCL3 6NH3은 전이 금속에 연결되거나 조정 된 이온 또는 분자를 함유하기 때문에 배위 화합물이라고한다. 그것들은 루이스 산-염기 복합체이기 때문에 복잡한 이온 또는 배위 복합체로도 알려져 있습니다. 리간드는 이들 복합체를 생성하기 위해 전이 금속 이온에 결합하는 이온 또는 분자이다 (라틴어로부터 "묶거나 결합하기 위해"). 배위 번호는 전이 금속 이온에 부착 된 리간드의 수를 나타냅니다. 배위 복합체는 코어 금속 원자가 비금속 원자 또는 리간드로 알려진 원자 그룹으로 둘러싸인 화학 구조이다. 유기 물질의 합성에 사용 된 염료 및 안료 및 촉매뿐만 아니라 비타민 B12, 헤모글로빈 및 엽록소는 조정 화합물의 예이다. 조정 화합물은 오늘날 야금, 약용 킬레이트 제, 화학 분석, 촉매 및 세제를 포함한 다양한 분야에서 사용됩니다. 합류 공유 결합을 통해 부착 된 금속 이온 코어 및 리간드를 갖는 복잡한 이온은 배위 화합물로 알려져있다.