주요 차이 - 가수 분해 대 수화
가수 분자는 물 분자를 분할하고 화합물의 화학적 결합을 파괴함으로써 화합물에 물 분자를 첨가하는 것입니다. 따라서, 가수 분해는 이중 분해 반응으로 간주된다. 수화라는 용어는 유기 화학 및 무기 화학에서 두 가지 다른 응용을 가지고 있습니다. 유기 화학에서는 알켄 또는 알키에 물 분자를 첨가하는 것입니다. 그러나 무기 화학에서, 수화는 물 분자를 절단하지 않고 물 분자의 연관성 또는 조합이다. 따라서 가수 분해와 수화의 주요 차이점은 가수 분자가 물 분자의 분할을 포함하는 반면, 수화에는 항상 물 분자의 분할을 포함하지는 않는다는 것입니다 .
주요 영역을 다루었습니다
1. 가수 분해 란 무엇입니까
- 정의, 다른 유형
2. 수화 란?
- 정의, 유기 및 무기 화학의 응용
3. 가수 분해와 수화의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :Alkene, Alkyne, Brønsted-Lowry 산-염기 이론, 분해 반응, 수화, 가수 분해, 용해도 상수

가수 분해 가란?
가수 분해는 반응물 중 하나로서 물과의 이중 분해 반응입니다. 다시 말해, 그것은 물 분자를 사용하여 분자에서 결합의 파괴입니다. 가수 분해 반응은 종종 가역적입니다. 가수 분해 반응에는 세 가지 주요 유형이 있습니다 :
- 산 가수 분해
- 베이스 가수 분해
- 염 가수 분해
물은 Brønsted-lowry acid 이론에 따라 산 또는 염기 역할을 할 수 있습니다 (이 이론에 따르면 산과 염기가 서로 반응 할 때 산은 그의 공액 염기를 형성하고, 기본은 양성자의 교환에 의해 그의 공액 산을 형성합니다). 물이 Brønsted-lowry 산 역할을하는 경우, 물 분자는 양성자를 기증합니다. 그것이 Brønsted-lowry베이스 역할을한다면, 물 분자는 양성자를 수용하여 히드로 늄 이온을 형성 할 수있다 (H 3 . 영형). 산 가수 분해 산 해리 반응과 유사합니다.

그림 1 :숙신성 무수물의 가수 분해
베이스 가수 분해 기본 해리 반응과 유사합니다. 여기서 물은 양성자를 기증하여 수산화 음이온 (OH)을 생성합니다. 따라서 물은 Brønsted-lowry 산 역할을합니다.
소금이 물에 용해되면 소금이 이온으로 분리됩니다. 이 해리는 용해도 상수에 기초한 완전한 해리 또는 불완전한 해리 일 수있다. 그러나 약산 또는 약한 염기의 염이 물에 용해 될 때, 물은 소금을 이온화하고 수산화 음이온 및 히드로 늄 양이온을 형성 할 수 있습니다. 소금은 또한 양이온과 음이온으로 분리됩니다. 이것은 염 가수 분해 로 알려져 있습니다 .
수화
수화는 물 분자가 물질과 결합되는 화학적 과정입니다. 유기 화학에서, 수화는 불포화 화합물, 알켄 또는 알킨에 물 분자를 첨가하는 것을 말한다. 그러나 무기 화학에서 수화는 물 분자와 화합물의 연관성을 말합니다.
유기 화학에서 물 분자는 불포화가 존재하는 지점에 추가됩니다. 여기서, 물 분자는 양성자 및 수산화물 음이온으로 절단된다. 수산화물 음이온은 더 많은 치환기를 갖는 탄소 원자와 결합을 형성한다. 양성자는 Markovnikov의 규칙에 따라 덜 치환 된 탄소와 결합됩니다. 불포화 유기 분자는 수화에 취약합니다.
무기 화학에서 수화는 물 분자와 무기 화합물의 연관성을 말합니다. 예를 들어, tio 2 의 생산을위한 설페이트 공정에서 Ilmenite 모래의 안료 (Fetio 3 ), FESO4는 부산물로 형성된다. 수화를 통한 결정화를 통한이 부산물. 여기에서 Feso 4 .7H 2 O는 FESO 4 의 반응에 의해 형성된다 물이 뒤 따른 다음 10C로 냉각됩니다. 그런 다음 feso 4 .7H 2 쉽게 제거 할 수있는 결정이 형성됩니다. 결정은 철 황산염 헵타 이드 레이트입니다.
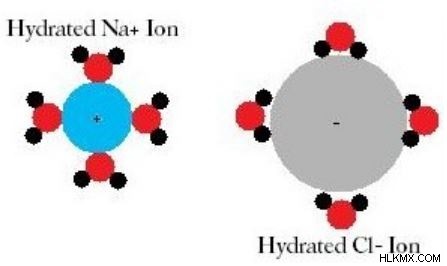
그림 2 :수화 된 나트륨 양이온 및 염화물 음이온
수화는 건조제로 발생하는 화학적 과정입니다. 건조제는 수증기를 흡수 할 수있는 화합물입니다. 또한, 수화 용어는 또한 나트륨 이온과 같은 염 이온의 용해를 설명하는데 사용된다. 소금이 물에 용해되면 소금은 양이온과 음이온에 분리됩니다. 이 양이온 및 음이온은 물 분자에 의한 이온의 수화로 인해 서로 분리된다. 여기서 물 분자는 소금 이온을 둘러싸고 수화라고합니다.
가수 분해와 수화의 차이
정의
가수 분해 : 가수 분해는 반응물 중 하나로서 물과의 이중 분해 반응입니다.
수화 : 수화는 물 분자가 물질과 결합되는 화학 공정입니다.
화학 결합
가수 분해 : 가수 분자는 물 분자에서 결합 절단으로 발생합니다.
수화 : 유기 분자의 수화는 결합 절단으로 발생하지만 무기 화합물에서는 절단이 일어나지 않습니다.
자연
가수 분해 : 가수 분해는 불포화 화합물로부터 포화 화합물을 형성한다.
수화 : 탈수 화합물로부터 수화 된 화합물을 형성한다.
결론
가수 분해와 수화는 학생들이 종종 혼동하는 두 가지 용어입니다. 가수 분해와 수화의 주요 차이점은 가수 분자가 물 분자의 분할을 포함하는 반면, 수화는 항상 물 분자의 분할을 포함하지 않는다는 것입니다.
참조 :
1.“가수 분해.” Encyclopædia Britannica, Encyclopædia Britannica, Inc., 2016 년 11 월 16 일, 여기에서 제공됩니다.
2. Chemistry LibreTexts, LibreTexts, 2016 년 7 월 21 일, 여기에서 구할 수 있습니다.
3.“가수 분해.” Wikipedia, Wikimedia Foundation, 2018 년 1 월 24 일, 여기에서 구입할 수 있습니다.
이미지 제공 :
1. –drdoht (talk) 00:26, 2016 년 2 월 21 일 (UTC)에 의한“숙시 닉 무수물의 가수 분해” - Commons Wikimedia
2를 통한 자신의 작업 (공개 도메인). KkeyShar의“수화” - Commons Wikimedia를 통한 자체 작업 (공개 도메인).