원자 척도에서 크기, 길이 및 각도와 같은 특정 매개 변수를 결정하는 것은 쉽지 않습니다. 이러한 매개 변수의 중요성 때문에 과학자들은 원자 수준에서 매개 변수를 추론하거나 계산하는 방법을 개발했습니다. 결합 순서 및 결합 길이는 한 쌍의 원자 사이의 결합의 유형과 강도를 나타내는 두 가지 중요한 파라미터입니다.
이 기사는
에 대해 설명합니다1. 채권 순서와 채권 길이는 무엇입니까
2. 채권 순서 및 채권 길이를 계산하는 방법
- 채권 주문 계산 방법
- 결합 길이를 계산하는 방법
채권 주문 및 채권 길이
채권 길이 및 채권 순서는 공유 결합과 관련된 두 가지 매개 변수입니다. 결합 순서는 두 원자와 결합 길이 사이의 화학적 결합의 수는 공유 결합 된 원자의 두 핵 사이의 거리입니다. 이 기사는 원자 수준에서 채권 순서와 채권 길이를 계산하는 방법을 설명합니다.
채권 순서를 계산하는 방법
결합 순서는 두 원자 사이의 화학적 결합 수입니다. 결합의 안정성을 나타냅니다. 공유 결합에서, 결합 순서는 공유 전자의 수이다. 예를 들어, 단일 결합에 의해 결합 된 한 쌍의 원자의 결합 순서는 하나 인 반면, 이중 결합에 의해 결합 된 원자 쌍의 결합 순서는 2이다. 제로 결합 순서는 원자 사이에 결합이 없음을 나타냅니다. 분자의 안정성은 결합 순서가 증가함에 따라 증가합니다. 공명 결합이있는 분자는 정수 일 필요는 없습니다. 2 개의 원자를 갖는 공유 화합물에서, 한 쌍의 원자 사이의 결합 순서는 먼저 루이스 구조를 그리는 다음 원자 사이의 결합 유형을 결정함으로써 결정된다 - 제로 결합, 단일, 이중 또는 트리플 결합. 예를 들어, 수소 가스의 결합 순서는 다음과 같이 결정됩니다.
- 루이스 구조를 그려
h :h
- 원자가 전자의 채권/쌍의 수를 결정하십시오
한 쌍의 전자, 따라서 결합 순서는 1입니다.
원자가 두 개 이상인 경우 결합 순서는 다음과 같이 결정됩니다. 예를 참조하십시오 :질산염 이온.
- 루이스 구조를 그립니다
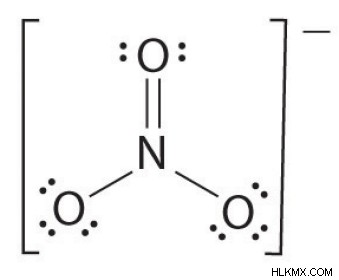
- 총 채권 수를 계산합니다 (질산염 이온에 따라 4)
- 개별 원자 사이의 결합 그룹 (암모니아에 따르면 3)
- 따라서 채권 주문 =총 채권 수/ 채권 그룹 수
=4/3
=1.33
따라서 질산염 이온의 결합 순서는 1.33
입니다.결합 길이를 계산하는 방법
결합 길이는 공유 결합 된 원자의 두 핵 사이의 거리입니다. 결합 길이는 일반적으로 0.1 내지 0.2 nm의 범위입니다. 두 개의 유사한 원자가 함께 결합되면 결합 길이의 절반을 공유 반경 라고합니다. . 결합 길이는 2 개의 원자의 결합 전자 수 또는 결합 순서에 따라 다릅니다. 결합 순서가 높을수록 채권 길이가 짧아지는 것은 긍정적으로 하전 된 핵의 강한 당기력으로 인한 것입니다. 결합 길이의 단위는 picometer 입니다 . 단일, 이중 및 삼중 채권에서, 결합 길이는
의 순서로 증가합니다. Triple Bond 전기 음성도는 전기성이 상이한 두 원자들 사이의 결합 길이를 계산하는 데 사용될 수 있습니다. 슈 메이커와 스티븐슨은 결합 길이를 계산하기 위해 다음의 경험적 공식을 제안했습니다. d a-b =r a + r b - 0.09 (x a - x b )
d a-b 두 원자 a와 b 사이의 결합 거리, r a 및 r b A와 B의 공유 반경 및
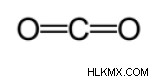
(x a - x b )은 A와 B의 전기 음성 차이입니다. 다른 메소드는 대략적인 결합 길이를 계산하는 데 사용됩니다. 이 방법에서, 공유 결합 유형을 결정하기 위해 첫 번째 루이스 구조가 그려진다. 그런 다음 Cordero et al 에 의해 수행 된 연구에 대한 차트* . 및 pyykkö 및 atsumi , 각 원자에 의해 제조 된 결합의 상응하는 반경이 결정된다. 그런 다음 결합 길이는 두 반경의 합을 취함으로써 결정됩니다. 예를 들어, 이산화탄소의 결합 길이를 결정할 때 첫 번째 루이스 구조가 그려집니다. 차트에 따르면, 탄소 이중 결합의 공유 반경은 67 피코 미터이고 산소 이중 결합의 반경은 57 피코 미터입니다. 따라서, 이산화탄소의 결합 길이는 약 124 피코 미터 (57 pm+ 67 pm)입니다.
*공유 차트는 여기에서 찾을 수 있습니다 Cordero, Beatriz, et al. "공유 반경이 재검토되었습니다." Dalton Transactions 21 (2008) :2832-2838. libreTexts. "채권 순서와 길이." 화학 libretexts. libretexts, 2016 년 12 월 5 일. 웹. 2017 년 1 월 10 일. Lister, Ted 및 Janet Renshaw. 고급 수준에 대한 화학 이해. N.P. :Nelson Thornes, 2000. Print. pratiyogita darpan. "전자 구조와 관련하여 요소의 특성." 경쟁 과학 비전 1998 년 8 월 :n. Pag. 인쇄. Pyykkö, Pekka 및 Michiko Atsumi. "요소 Li -E112의 분자 이중 결합 공유 반경." 화학-유럽 저널 15.46 (2009) :12770-12779.