주요 차이 - 금속 대 비금속 대 금속성
주기적인 요소 테이블은 지구에서 발견 된 모든 요소를 나타냅니다. 이 금속은 특성의 유사성에 따라 다른 범주로 분류 될 수 있습니다. 그러나 이러한 요소를 분류하는 주요 방법은 그들이 표시하는 금속 특성의 정도에 따른 것입니다. 요소는이 분류에 따라 금속, 비금속 및 금속성으로 분류됩니다. 금속은 일반적으로 단단하고 반짝이고, 냉담하고, 가단성 및 연성이 있으며, 전기 및 열전도율이 우수한 요소입니다. 비금속은 금속의 특성이없는 요소입니다. 메탈 로이드는 금속과 비금속 모두의 중간 특성을 갖는 요소입니다. 이것은 금속 비금속과 금속성의 주요 차이점입니다.
주요 영역을 다루었습니다
1. 금속이란?
- 정의, 속성, 예
2. 비금속이란 무엇입니까
- 정의, 속성, 예
3. 메탈 로이드
- 정의, 속성, 예
4. 금속 비금속과 메탈 로이드의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :연성, 가상, 금속, 메탈 로이드, 비금속

금속
금속은 가장 높은 수준의 금속 거동을 갖는 요소입니다. 금속은 주기율표의 왼쪽에 있습니다. 그들은 광택이나 빛으로 알려진 특징적인 금속성 모양을 가지고 있습니다. 연성과 가단성은 금속의 주요 특징입니다. 가단성은 압력과 연성하에 변형되는 금속의 능력을 말합니다. 와이어와 같은 구조물로 끌리는 능력을 말합니다.
금속은 일반적으로 실온에서 고체입니다. 그러나 수은은 예외입니다. 수은은 금속 요소이지만, 다른 모든 금속은 일반적으로 더 높은 융점을 가지기 때문에 실온에서 액체입니다. 다른 금속 원자와 달리, 수은 원자는 서로 전자를 공유 할 때 약하므로 상호 작용이 약합니다. 따라서, 수은 원자가 쉽게 빠져 나올 수 있으므로 융점이 낮아집니다.

그림 1 :에펠 탑 - 금속으로 만든.
금속은 전기 전기에 참여할 수있는 전자를 쉽게 잃어 버리기 때문에 우수한 열과 전기 도체입니다. 다시 말해, 금속에는 전자가 유리가 있습니다. 금속은 일반적으로 습한 조건과 바닷물의 존재 하에서 부식을 겪습니다.
주기율표에서 금속 요소는 모든 s, p, d 및 f 블록에서 발견됩니다. 금속은 가장 바깥 쪽 S와 P 궤도에 전자 수가 적습니다 (금속 제외). 일반적으로 금속은 양이온을 형성 할 수 있으며 산화 수는 거의 항상 양수 값입니다. 금속은 또한 매우 낮은 전기 음성 값을 나타내며 이온 성 화합물을 형성합니다.
비금속
비금속은 금속성 특성이 적거나 전혀없는 요소입니다. 비금속은 금속과 금속성의 특성보다 매우 뚜렷한 특성을 가지고 있습니다. 일반적으로 비금속은 금속 외관이 없기 때문에 둔한 외관을 가지고 있습니다.
금속과 달리 비금속은 가단성이 없거나 연성이 아닙니다. 그들은 부서지기 쉽다. 비금속은 전기와 열의 열악한 도체입니다. 금속에 비해 비금속은 밀도가 낮습니다. 비금속의 대부분은 가스입니다. 그러나 액체와 고형물도 있습니다.

그림 2 :다이아몬드- 탄소로 만든; 비금속
비금속은 주기율표의 오른쪽에 포함됩니다. 이 비금속은 S 및 P 블록에 포함됩니다. 이들 요소는 가장 바깥 쪽 S와 P 궤도에 많은 수의 전자를 갖는다. 그들은 자유 전자가 거의 없거나 거의 없습니다.
비금속의 녹는 점이 매우 낮습니다. 그들은 전자를 얻어 음이온을 형성하는 경향이 있습니다. 그들은 공유 화합물을 형성합니다. 비금속의 산화 수는 양의 또는 음성 일 수 있습니다. 전기 음성은 비금속에서 매우 높습니다.
메탈 로이드
메탈 로이드는 금속 거동 정도가 낮은 요소입니다. 메탈 로이드는 일부 금속성 특성과 비금속 특성을 보여줍니다. 메탈 로이드의 모양은 둔하거나 반짝일 수 있습니다. 우수한 열 및 전기 도체는 아니지만 메탈 로이드는 열과 전기를 수행 할 수 있습니다.
메탈 로이드의 주요 적용은 반도체 생산에 있습니다. 모든 메탈 로이드는 실온에서 고체입니다. 메탈 로이드의 밀도는 금속과 비금속 사이에 있습니다. 그들은 부서지기 쉽다. 메탈 로이드는 주기율표의 P 블록에 배치됩니다. 이 요소는 주기율표에서 금속과 비금속 사이에 위치합니다. S와 P 궤도의 전자 수는 중간 수입니다.

그림 3 :메탈 로이드로 만든 반도체
메탈 로이드는 공유 결합을 형성합니다. 따라서, 금속성은 공유 화합물에서 발견된다. 메탈 로이드는 실온에서 고체이기 때문에 녹는 점이 높습니다. 수용액에서 메탈 로이드는 음이온을 형성하고 양성 또는 음성 산화 수를 나타냅니다.
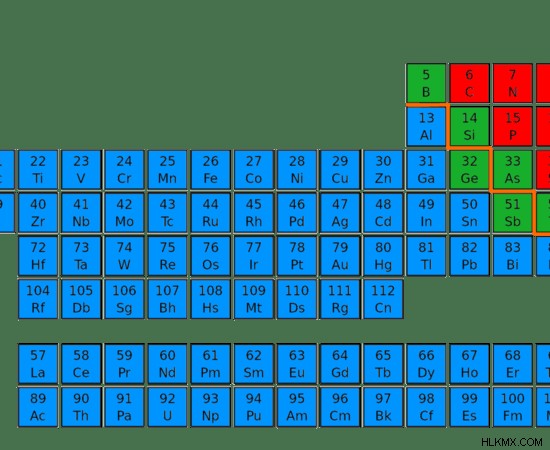
그림 4 :주기성 테이블의 금속 (파란색), 비금속 (빨간색) 및 금속성 (녹색)의 위치
금속 비금속과 금속의 차이
정의
금속 : 금속은 금속 거동이 가장 높은 요소입니다.
비금속 : 비금속은 금속 특성이 적거나없는 요소입니다.
메탈 로이드 : 금속성은 금속 거동이 낮은 요소입니다.
주기율표에서의 위치
금속 : 금속은 주기율표의 왼쪽에 있습니다.
비금속 : 비금속은 오른쪽에서 주기성 테이블에 있습니다.
메탈 로이드 : 메탈 로이드는 주기율표 중간에 있습니다.
주기성 테이블의 블록
금속 : 금속은 s, p, d 및 f 블록에 있습니다.
비금속 : 비금속은 s 및 p 블록에서 발견됩니다.
메탈 로이드 : 메탈 로이드는 P 블록에서 발견됩니다.
외관
금속 : 금속은 반짝이는 외관을 가지고 있습니다.
비금속 : 비금속은 둔한 모양을 갖습니다.
메탈 로이드 : 메탈 로이드는 칙칙하거나 반짝이는 외관을 가지고 있습니다.
가용성과 연성
금속 : 금속은 가단성과 연성을 보여줍니다.
비금속 : 비금속은 가단성과 연성을 나타내지 않습니다.
메탈 로이드 : 메탈 로이드는 가변성과 연성을 나타내지 않습니다.
열 및 전기 전도도
금속 : 금속의 열 및 전기 전도도는 매우 높습니다.
비금속 : 비금속의 열 및 전기 전도도는 매우 낮습니다.
메탈 로이드 : 메탈 로이드의 열 및 전기 전도도는 양호하지만 금속보다 적습니다.
전기 음성
금속 : 금속은 전기 음성이 매우 낮습니다.
비금속 : 비금속은 매우 높은 전기 음성을 나타냅니다.
메탈 로이드 : 메탈 로이드는 전기 음성의 중간 값을 갖는다.
결론
금속, 비금속 및 금속성은 지구에서 발견되는 요소입니다. 이러한 요소의 대부분은 다양한 응용 분야에서 사용됩니다. 금속 비금속과 금속성의 주요 차이점은 금속이 가장 높은 금속 거동을 나타내고 비금속은 금속 거동을 나타내지 않는 반면, 금속성은 어느 정도의 금속 거동을 나타냅니다.
.참조 :
1. Helmenstine, Ph.D. 앤 마리. "금속 비금속 및 금속성 - 주기적 표." 사고. N.P., N.D. 편물. 여기에서 사용할 수 있습니다. 2017 년 6 월 26 일.
2. libretexts. "금속, 비금속 및 금속성." 화학 libretexts. LibreTexts, 2016 년 10 월 25 일. 웹. 여기에서 사용할 수 있습니다. 2017 년 6 월 26 일.
3. Boudreaux, Kevin A.“금속, 비금속 및 금속성.” 주기율표의 일부. N.P., N.D. 편물. 여기에서 사용할 수 있습니다. 2017 년 6 월 26 일.
이미지 제공 :
1. Pixabay
2를 통한 2267674 ″ (공개 도메인). Steve Jurvetson의 "Apollo Synthetic Diamond" - Commons Wikimedia
3을 통해 (CC x 2.0). Nixdorf의“National Semiconductor 8250a”-Commons Wikimedia
4를 통한 OWN OUT (CC BY-SA 3.0). Riccardo Rovinetti의“Metalli, Semimetalli, Non-Metalli”-Commons Wikimedia를 통해 자신의 작업 (CC By-SA 3.0)







