주요 차이 - 황과 황산염
지구상의 유황의 풍부는 0.042%로 결정되었습니다. 산소와 실리콘과 같은 요소에 비해 아주 적은 양이지만 지구상에서 가장 풍부한 13 가지 요소입니다. 황산염은 황 원자로 구성된 음이온입니다. 그러나 황과 황산염 사이에는 뚜렷한 차이가 있습니다. 황과 황산염의 주요 차이점은 황이 요소이고 황산염은 음이온이라는 것입니다.
주요 영역을 다루었습니다
1. 유황이란?
- 화학적 및 물리적 특성, 동반 로프
2. 황산염이란?
- 화학 및 물리적 특성
3. 황과 황산염의 차이는 무엇입니까
- 주요 차이점 비교
주요 용어 :동종, 비금속, 단일 소화 된 황, 사방 정광 황 <>, 마름모꼴 황, 실리콘, 황산염, 황, 원자가 
유황이란 무엇입니까
sulfur는 요소입니다. 황의 원자 수는 기호 "S"가있는 16이고 황의 전자 구성은 1S2S2P3S3p입니다. 이 요소의 궤도를 함유하는 가장 바깥 쪽 전자는 p 궤도입니다. 따라서 황은 P 블록으로 그룹화됩니다. 황의 전자 구성에 따르면 황의 원자가는 6입니다. 즉, 그 주위에 최대 6 개의 결합을 형성 할 수 있습니다. 따라서 황은 산화 상태를 최대 +6까지 가질 수 있습니다. 그러나 때때로 황은 p 궤도를 채우기 위해 2 개의 전자를 더 많이 얻은 다음 산화 상태 -2를 얻을 수 있습니다.
.일반적으로 황은 실온에서 고체로 발견됩니다. 그러나이 고체는 순수한 황 원자를 포함하지 않습니다. 대부분의 경우 황 고체는 s 8 로 만들어집니다. 단위. 이것을 황 결정이라고합니다. 하나의 s 8 단위는 8 개의 황 원자로 구성됩니다. 주기적 구조이며 매우 안정적입니다. 단단한 황은 밝은 노란색으로 나타납니다.

그림 1 :황 결정
황의 녹는 점은 약 115c입니다. 황의 원자 질량은 32 g/mol입니다. 유황은 비금속입니다. 황 고체는 결정으로 만들어 졌기 때문에 취성 구조입니다. 그러나 황은 물에 불용성입니다.
sulfur에는 여러 개의 동종이 있습니다. 황 원자의 조성 및 구조에 따라 이러한 황의 이들 동화물은 서로 다릅니다. 일반적인 동화물 중 일부는 다음과 같습니다.
황의 동종
오피카 정열 황
s 8 장치는 "크라운"구조에 있습니다.
마름모꼴 황화
이것은 안정적인 고체이며 s 8 로 구성됩니다. 단위. s 8 의 형상 단위는 마름모꼴입니다.
모노 클리닉 황
이것들은 바늘 모양의 구조입니다.
그러나 황의 샘플을 천천히 그리고 꾸준히 가열하여 다른 할당수로부터 하나의 할당수를 쉽게 얻을 수 있습니다.
설페이트
설페이트는 음이온이며 황 원자와 4 개의 산소 원자로 구성됩니다. 이 음이온의 전반적인 전하는 -2입니다. 설페이트의 분자 공식은 So 4 입니다 . 그곳에서, 2 개의 산소 원자가 이중 결합을 통해 황 원자에 결합되고, 다른 2 개는 단일 결합을 통해 황에 결합된다. 설페이트에서 황의 산화 상태는 +6입니다. 황이 가질 수있는 최대 산화 상태입니다. 따라서 황산염은 산화 반응을 겪을 수 없습니다.
그러나 황산염의 결합 길이가 실험적으로 결정되면 모든 결합 길이가 동일하다는 것이 밝혀졌습니다. 따라서 설페이트에는 공명 구조가 있음을 나타냅니다.
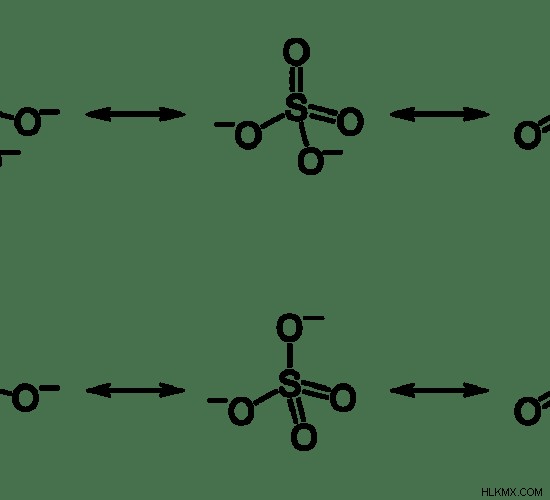
그림 2 :황산염의 공명 구조
설페이트 음이온의 몰 질량은 약 96 g/mol입니다. 대부분의 황산염 화합물은 물에 용해됩니다. 그러나 일부 황산염의 용해도는 가난하거나 전혀 용해되지 않습니다. 예를 들어, Baso 4 (바륨 설페이트)는 물에 불용성이 있습니다. 일부 황산염 화합물은 무색이며 일부는 물에있을 때 매우 화려합니다. 예를 들어, cuso 4 (구리 황산염) 수용액에있을 때 밝은 청색이지만 물 분자가없는 경우 흰색입니다.
황과 설페이트의 차이
정의
황 : 유황은 기호가있는 요소입니다.
설페이트 : 황산염은 음이온 (s)과 4 개의 산소 원자 (O)로 구성된 음이온입니다.
질량
황 : 황의 원자 질량은 약 32 g/mol.
입니다설페이트 : 설페이트의 몰 질량은 약 96 g/mol.
입니다기하학
황 : 황의 기하학은 사방 정계, 마름모꼴 또는 단일 클린 일 수 있습니다.
설페이트 : 황산염의 기하학은 사면체입니다.
구성
황 : 고체 황은 s 8 로 구성됩니다 단위.
설페이트 : 황산염은 황과 산소 원자로 구성됩니다.
용융점
황 : 황의 용융점은 약 115C입니다.
설페이트 : 설페이트의 용융점은 그것에 결합 된 양이온에 의존한다.
전하
황 : 유황은 중립적으로 하전됩니다.
설페이트 : 황산염은 음으로 하전됩니다.
결론
황 원자는 다양한 유형의 화합물이나 황 동화 로프에서 찾을 수 있습니다. 유황 동종 트로프는 황 원자로 만 구성되는 반면 황 함유 화합물은 다른 많은 원소로 구성됩니다. 황과 황산염의 주요 차이점은 황산은 원소이고 황산염은 음이온이라는 것입니다.