주요 차이 - 원자가 vs 공유
원자는 물질의 빌딩 블록입니다. 각각의 모든 원자는 핵과 전자 구름으로 구성됩니다. 핵은 원자의 핵심이며 전자 구름으로 둘러싸여 있습니다. 전자 구름의 개념은 전자의 위치의 확률에 따라 진화된다. 이것은 전자가 항상 핵 주위에 움직이고 있음을 의미합니다. 이 경로를 궤도 또는 껍질이라고합니다. 전자는이 궤도를 따라 움직이고 있다고합니다. 원자가 및 공유는 원자에 존재하는 전자 수와 관련된 두 가지 항입니다. 원자가와 공동의 주요 차이점은 원자가는 원자가 자체를 안정화시키기 위해 원자가 잃거나 얻는 전자의 수이며, 공유는 빈 궤도를 사용하여 원자가 형성 할 수있는 최대 공유 결합 수입니다. .
주요 영역을 다루었습니다
1. 원자가
- 정의, 속성, 예
2. 공동
- 정의, 속성, 예
3. 원자가와 공유의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :원자, 공동, 공유 결합, 전자, 궤도, 쉘, 원자가 
원자가는 무엇입니까
원자가는 스스로 안정화하기 위해 원자가 잃거나 얻는 전자의 수로 정의 될 수 있습니다. 원자의 가장 바깥 쪽 궤도에있는 전자는 원자가 전자로 알려져 있습니다. 때로는 원자가 전자의 수는 해당 요소의 원자가로 간주됩니다. 예를 들어, 수소 원자가 1 전자를 잃거나 얻어 안정화 될 수 있기 때문에 수소 (H)의 원자가는 1이다. 염소 원자는 가장 바깥 쪽 궤도에 7 개의 전자 (원자가 전자의 수는 7)를 가지지 만 1 개 더 전자를 얻으면 더 안정적인 아르곤 (AR)의 고귀한 가스 전자 구성을 얻을 수 있습니다. 7 개의 전자를 잃지 않고 하나의 전자를 얻는 것은 쉽기 때문에 염소의 원자가는 1으로 간주됩니다.
요소의 전자 구성은 특정 요소의 원자가를 제공합니다. 다음 표는 계곡이있는 일부 요소를 보여줍니다.
|
요소
|
전자 구성
|
옥켓 규칙을 준수하기 위해 얻거나 방출 해야하는 전자
|
원자가
|
|
나트륨 (NA)
|
1S2S2P3S
|
(-) 1
|
1
|
|
칼슘 (ca)
|
1S2S2P3S3P4S
|
(-) 2
|
2
|
|
질소 (n)
|
1S2S2p
|
(+) 3
|
3
|
|
염소 (CL)
|
1S2S2P3S3p
|
(+) 1
|
1
|
위의 표는 일부 요소의 원자가를 보여줍니다. 그곳에서 (-) 마크는 안정화되기 위해 제거 해야하는 전자의 수를 나타 냈습니다. (+) 마크는 안정화되기 위해 얻어야하는 전자의 수를 나타냅니다.
그림 1 :주기적인 요소 테이블
그 외에도주기적인 요소 테이블은 요소의 원자가에 대한 아이디어를 줄 수 있습니다. 그룹 1 요소는 항상 원자가 1을 가지며 그룹 2 요소의 경우 밸런스는 2입니다.
공유
공유는 빈 궤도를 사용하여 원자가 형성 할 수있는 최대 공유 결합 수입니다. 공유는 원소의 원자가 전자의 수에 따라 다릅니다. 예를 들어, 수소에 존재하는 원자가 전자의 수는 1이고, 수소의 공유는 1이기 때문에 다른 원자와 공유 할 수있는 전자가 하나뿐이므로 공유 결합을 형성합니다.
. 탄소와 같은 요소가 고려되면 탄소의 전자 구성은 1S2S2P입니다. 탄소의 원자가 전자의 수는 4이며 비어있는 p 궤도가 있습니다. 따라서, 2s 궤도의 2 개의 S 전자는 분리되어 이러한 p 궤도에 포함될 수있다. 그런 다음 탄소에는 4 개의 짝을 이루지 않은 전자가 있습니다. 따라서, 탄소는 공유 결합을 형성하기 위해 4 개의 전자를 공유 할 수있다. 따라서, 탄소의 공동은 4입니다. 탄소 원자가 가질 수있는 최대 공유 결합 수입니다. 이것은 아래에 표시된 궤도 다이어그램으로 설명됩니다.
탄소의 원자가 전자; 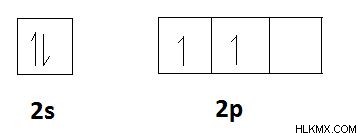
빈 궤도에 전자의 확산; 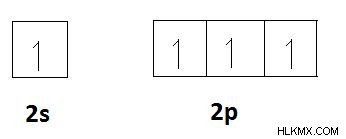
이제 공유 결합을 형성하기 위해 다른 원자와 공유 할 탄소가 4 개의 짝을 이루지 않은 전자가 있습니다.
원자가와 공유의 차이
정의
원자가 : 원자가 자체를 안정화시키기 위해 원자가 잃거나 얻을 수있는 전자의 수입니다.
공유 : 공유는 빈 궤도를 사용하여 원자가 형성 할 수있는 최대 공유 결합 수입니다.
원자가 전자와의 관계
원자가 : 원자가는 원자가 전자의 수와 같을 수 있습니다.
공유 : 공유는 원자가 전자의 수에 따라 다릅니다.
빈 궤도
원자가 : 원자가는 빈 궤도를 채우는 데 필요한 전자의 수를 제공합니다.
공유 : 공유는 원자에 존재하는 빈 궤도의 수에 따라 다릅니다.
본딩 유형
원자가 : 이온 성 또는 공유 결합을 형성 할 수있는 요소에 대해 원자가가 주어질 수 있습니다.
공유 : 공유 결합을 형성 할 수있는 요소에 대해서만 공유가 주어질 수 있습니다.
결론
원자가는 때때로 원자의 원자가 전자 수와 같을 수 있지만 대부분은 다릅니다. 그러나, 공유는 원자의 원자가 전자의 수에 전적으로 의존합니다. 원자가 전자는 원자가 가질 수있는 공유 결합의 수를 결정하기 때문입니다. 따라서 원자가와 공유의 차이를 아는 것이 중요합니다.