주요 차이 - 불활성 가스 vs 고귀한 가스
물질은 고체 상태, 액체 상태 및 기체 상태로 알려진 세 가지 주요 물리적 상태에 존재할 수 있습니다. 기체 상태에는 원소 또는 화합물 인 가스가 포함됩니다. 그러나 가스는 미세한 질량이있는 작은 입자로 구성됩니다. 이 기체 입자 사이에 존재하는 인력은 매우 적습니다. 따라서, 이들 입자는 입자들 사이에서 발생하는 충돌로 인해 항상 움직입니다. 가스는 반응성 가스 및 불활성 가스로 발견됩니다. 고귀한 가스는 비활성 가스의 한 유형입니다. 불활성 가스와 고귀한 가스의 주요 차이점은 불활성 가스가 화학 반응을 겪지 않는 반면 고귀한 가스는 특정 조건에서 화학 반응을 겪을 수 있다는 것입니다.
주요 영역을 다루었습니다
1. 불활성 가스는 무엇입니까
- 정의, 속성, 예
2. 고귀한 가스는 무엇입니까
- 정의, 속성, 예
3. 불활성 가스와 고귀한 가스의 관계는 무엇입니까
- 불활성 가스 및 고귀한 가스
4. 불활성 가스와 고귀한 가스의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :불활성 가스, 고귀한 가스, 수소, 헬륨, 네온, 크세논, 질소 
불활성 가스가 무엇인가
불활성 가스는 화학 반응을 겪지 않는 화합물입니다. 이들은 비 반응성 가스입니다. 불활성 가스는 원소 일 수 있거나 화합물로 존재할 수 있습니다. 아르곤은 원소 불활성 가스의 좋은 예입니다. 질소는 대부분 불활성 가스로 간주됩니다. 그것은 2 개의 질소 원자로 구성된 화합물입니다.
불활성 가스의 비 반응성 거동은 완성 된 원자가 껍질로 인해 발생합니다. 다시 말해, 이들 가스의 원자의 가장 바깥 전자 껍질은 완전히 채워진다. 따라서, 모든 전자 쉘을 채우거나 완전한 원자가 껍질을 얻기 위해 가장 바깥 쪽 쉘에서 전자를 제거함으로써 안정적이되기 위해 다른 모든 원자가 다른 화학 종과 반응하기 때문에 다른 화학 종과 더 반응 할 필요가 없습니다.
.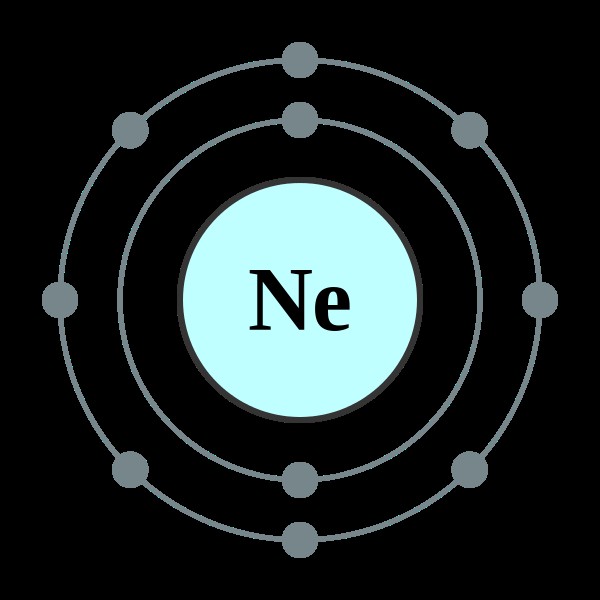
그림 01 :네온의 원자 구조
네온은 불활성 가스입니다. 그것은 네온 원자로 구성됩니다. 네온은 가장 바깥 쪽 쉘이 전자로 완전히 채워져 있기 때문에 화학 반응을 겪을 수 없습니다.
불활성 가스는 화학 반응을 피해야하는 상황에서 유용합니다. 예를 들어, 식품 패키지에 불활성 가스를 사용하는 것은 박테리아 성장을 방지하기 때문에 안전합니다. 불활성 가스는 오염을 피하기 위해 텅스텐을 용접으로 보호하는 데 사용됩니다.
고귀한 가스는 무엇입니까
고귀한 가스는 주기율표의 그룹 18의 화학 요소입니다. 따라서 6 개의 고귀한 가스가 있습니다. 그들은 그 (헬륨), NE (네온), AR (아르곤), KR (크립톤), XE (XEON) 및 RN (Radon)입니다. 그들은 다른 화학 요소들 사이에서 반응성이 없거나 매우 낮은 반응성을 나타냅니다. 이 요소의 원자가 원소의 원자가 완전히 가득 차 있었기 때문입니다. 헬륨은 단 하나의 궤도를 가지고 있습니다. 따라서이 궤도에서 최대 2 개의 전자를 갖습니다. 다른 요소에는 8 개의 전자로 가득 찬 S 및 P 쉘이 있습니다.
이 요소들은 매우 반응하지 않습니다. 그러나 극한의 조건에서는 화합물로 만들 수 있습니다. 이 모든 가스는 정상적인 조건 하에서 모노 토미 가스입니다. 극한 조건에서도 헬륨과 네온은 화학적 결합에 참여하지 않습니다. 그러나, 아르곤, 크립톤, 크세논은 약하게 반응하며 화학적 결합을 형성하는 화합물에 참여할 수있다. 라돈은 방사성 요소로 발견됩니다.
Xenon에서 형성된 화합물에 대한예 :
크세논 헥사 플루오 라이드 (xef 6 )) 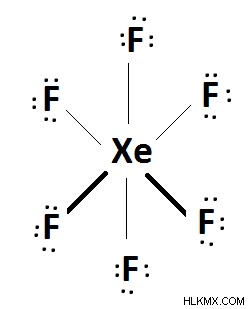
Xenon Tetrafluoride (xef 4 )) 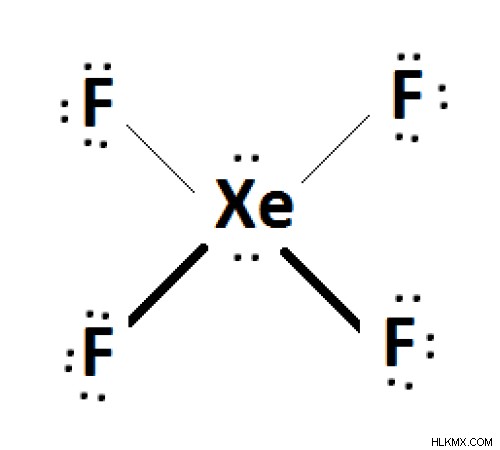
크세논 디 플루오 라이드 (xef 2 )
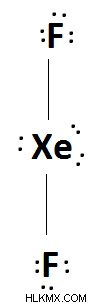
krypton은 크세논과 같은 불소를 형성 할 수 있습니다. 또한 크립톤은 수소, 탄소 및 구리와 같은 전이 금속과 같은 다른 비금속에 화학적으로 결합 될 수 있습니다.
불활성 가스와 고귀한 가스의 관계
모든 고귀한 가스는 표준 온도 및 압력 조건에서 불활성 가스로 간주됩니다. 그러나 모든 불활성 가스는 고귀한 가스가 아닙니다.
불활성 가스와 고귀한 가스의 차이
정의
불활성 가스 : 불활성 가스는 화학 반응을 겪지 않는 화합물입니다.
고귀한 가스 : 고귀한 가스는 주기율표의 그룹 18의 화학 요소입니다.
가스 입자
불활성 가스 : 불활성 가스는 원자 또는 분자로 구성 될 수 있습니다.
고귀한 가스 : 고귀한 가스는 원자로만 구성됩니다. 분자가 없습니다.
화학 반응성
불활성 가스 : 불활성 가스는 화학적으로 비 반응성입니다.
고귀한 가스 : 고귀한 가스는 일반적으로 반응하지 않지만 극한 조건에서는 반응 할 수 있습니다.
요소
불활성 가스 : 불활성 가스에는 모든 고귀한 가스와 다른 비활성 기체 화합물이 포함됩니다.
고귀한 가스 : 고귀한 가스는주기 테이블의 그룹 18의 요소입니다.
결론
불활성 가스와 고귀한 가스는 정상적인 조건에서 반응하지 않습니다. 그러나 고귀한 가스는 특정 조건에서 화학적 결합을 만들 수 있습니다. 이들 원자 또는 화합물은 전자로 완전히 채워진 가장 바깥 쪽 껍질로 구성되기 때문에 극한의 조건이 필요하다. 그러나 모든 고귀한 가스는 불활성 가스이지만 모든 불활성 가스는 고귀한 가스가 아닙니다. 이것은 불활성 가스와 고귀한 가스의 차이입니다.







