주요 차이 - 비틀 거리는 vs 이클립스 형태
형태라는 용어는 분자의 다른 형태의 투영을 설명합니다. 다시 말해, 분자가 구부러 질 수있는 다른 위치에 대한 이름입니다. 분자에서 원자의 배열은 분자의 변형에 큰 영향을 미칩니다. 분자의 안정성은 변형 형태가 낮은 경우 높다. 알칸 입체 화학에서 일반적으로 사용되는 뉴먼 투영은 전면 방향으로 C-C 결합을 통과 할 때 분자의 형태를 보여줍니다. 비틀 거리는 형태와 이클립스 형태는 원자의 공간 배열을 보여주는 두 가지 유형의 뉴먼 투영이다. 비틀 거리는 형태와 이클립스 형태의 주요 차이점은 비틀 거리는 입체 형태가 잠재적 에너지가 낮은 반면, 이클립스 형태는 최대 잠재적 에너지를 가지고 있다는 것입니다.
주요 영역을 다루었습니다
1. 비틀 거리는 형태
- 정의, 구조 및 예
2. 일식 형태
- 정의, 구조 및 예
3. 비틀 거리는 형태와 일식 형태의 차이점은 무엇입니까
- 주요 차이점 비교
핵심 용어 :알칸스, 이하 각도, 이클립스 형태, 에탄, 뉴먼 투영, 잠재적 에너지, 비틀 거리는 형태, 변형 
비틀 거리는 형태
비틀 거리는 형태는 분자에서 원자 또는 원자 그룹의 배열입니다. 이 형태는 원자 또는 원자 그룹이 결합 전자 쌍 사이의 반발이 최소화되는 방식으로 위치되기 때문에 분자에 낮은 변형을 제공한다. 비틀 거리는 형태의 원자 사이에 공간이있어 원자 사이의 반발이 최소화되도록합니다. 따라서 가장 안정적인 형태입니다. 이것은 비틀 거리는 형태의 분자가 다른 가능한 형태와 비교할 때 낮은 잠재적 에너지를 가지고 있음을 나타냅니다.
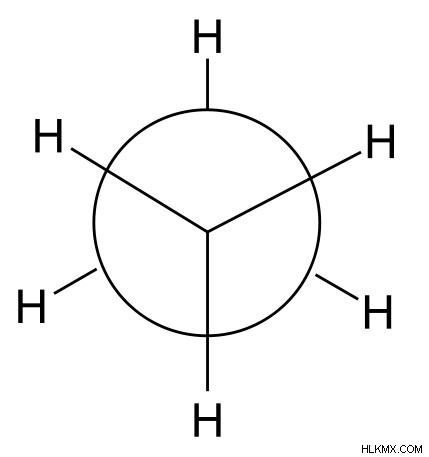
그림 1 :비틀 거리는
에탄의 형태
위의 이미지는 에탄의 비틀 거리는 형태를 보여줍니다. 비틀 거리는 형태는 에탄에 대한 다른 가능한 형태 중에서 가장 안정적인 형태입니다. 이는 C-H 결합의 결합 전자 쌍 사이의 최소 반발 때문입니다.
이클립스 형태
eclipsed 형태는 분자에서 원자 또는 원자 그룹의 배열이 0 Dihedral 각도로 생성됩니다. 따라서이 형태의 안정성은 매우 낮습니다. 이클립스 형태에 원자 또는 원자 그룹 사이에 공간이 없기 때문에, 결합 전자 쌍 사이에 높은 반발이 있습니다. 따라서, 이클립스 형태는 덜 안정적이다. 이 배열에서, 원자들 사이의 변형은 매우 높다. 이 형태는 불안정하기 때문에이 분자는 잠재적 에너지가 높음을 나타냅니다.
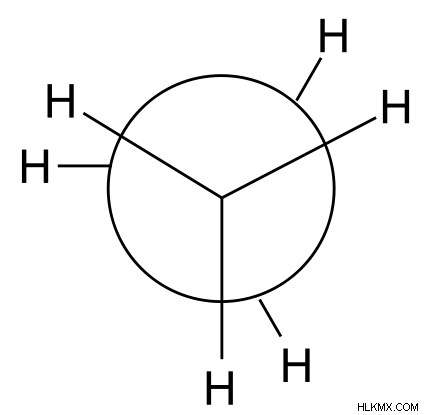
그림 2 :에탄의 일식 형태
위의 이미지는 에탄의 일식 형태의 스케치를 보여줍니다. 그러나 그것은 실제 구조가 아닙니다. 실제 구조는 다른 3 개의 원자가 전면 3 개의 원자에 덮여 있기 때문에 3 개의 원자만을 보여줍니다.
스aggered와 일식 형태의 차이
정의
비틀 거리는 형태 : 비틀 거리는 형태는 분자에서 원자 또는 원자 그룹의 배열로, 60 개의 이하 각도를 초래합니다.
eclipsed 형태 : 이클립스 형태는 분자에서 원자 또는 원자 그룹의 배열로, 0 Dihedral 각도를 초래한다.
잠재적 에너지
비틀 거리는 형태 : 비틀 거리는 형태는 잠재적 에너지가 낮습니다.
이클립스 형태 : 이클립스 형태는 최대 잠재적 에너지를 가지고 있습니다.
스트레인
비틀 거리는 형태 : 비틀 거리는 형태는 낮은 변형 구조입니다.
이클립스 형태 : 일식 형태는 높은 변형 구조입니다.
안정성
비틀 거리는 형태 : 비틀 거리는 형태의 안정성은 높다.
이클립스 형태 : 일식 형태의 안정성은 낮다.
결론
비틀 거리는 형태와 일식 형태는 뉴먼 투영의 두 가지 주요 형태입니다. 이들 구조는 전면 방향으로부터 탄소 골격을 통해 볼 때 분자의 구조를 제공한다. 비틀 거리는 형태와 이클립스 형태의 주요 차이점은 비틀 거리는 형태가 잠재적 에너지가 낮고 일식 형태는 최대 전위 에너지를 가지고 있다는 것입니다.