주요 차이 - 과산화수소 대 과산화수소
과산화물은 산소-산소 단일 결합으로 구성된 화합물입니다. 이것은 음이온의 형태 또는 분자의 다른 원자 사이에있을 수 있습니다. 과산화수소는 발견 될 수있는 가장 간단한 과산화물입니다. 2 개의 수소 원자와 2 개의 산소 원자로 구성됩니다. 이 두 산소 원자는 단일 결합을 통해 서로 결합됩니다. 수소 원자 대신 산소-산소 결합에 결합 된 상이한 원자가있을 때,이 단일 결합에 결합 된 원자 또는 원자 그룹의 유형에 따라 명명된다. 그러나, 이러한 과산화물은 화학적 및 물리적 특성에서 서로 다릅니다. 과산화수소와 과산화수소의 주요 차이점은 퍼 옥사이드가 이온 성 화합물 또는 공유 화합물 일 수 있지만 과산화수소는 공유 화합물이라는 것입니다.
주요 영역을 다루었습니다
1. 과산화수소
- 정의, 속성, 사용
2. 과산화수소 수소
- 정의, 속성, 사용
3. 과산화수소와 과산화수소의 유사점은 무엇입니까
- 일반적인 기능의 개요
4. 과산화수소와 과산화수소의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :공유 화합물, 과산화수소, 이온 성 화합물, 산소, 과산화물 
과산화물
과산화물은 산소-산소 단일 결합으로 구성된 화합물입니다. 따라서, 과산화물 화합물을 식별하는 주요 특징은이 O-O 공유 결합의 존재이다. 때때로,이 결합은 이온 성 화합물에서 음이온으로 관찰 될 수있다. 그런 다음 기호로 o 2 로 제공됩니다 . 이것을 과산화물 음이온이라고합니다. O-O 결합이 공유 화합물에서 발견되면이를 퍼 옥소 그룹 또는 퍼 옥사이드 그룹이라고합니다.
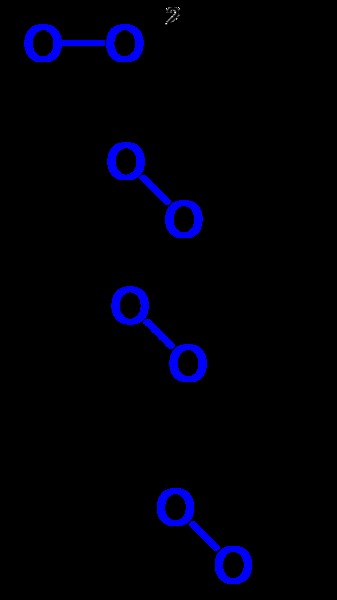
그림 1 :위의 예에서, 푸른 색의 결합은 과산화물 그룹을 보여줍니다.
퍼 옥사이드 그룹에서 하나의 산소 원자의 산화 상태는 -1입니다. 일반적으로 산소는 산화 상태 0 또는 -2를 보여주는 것을 선호합니다. 그러나 두 개의 산소 원자가 서로 결합되기 때문에 하나의 산소 원자는 -1 산화 상태를 가져옵니다. 과산화물 음이온에서, 하나의 산소 원자는 음이온의 전체 전하가 -2이기 때문에 -1 전하를 갖는다.
이온 퍼 옥사이드는 양이온으로서 알칼리 금속 이온 또는 알칼리성 지구 금속 이온에 결합 된 과산화물 음이온으로 구성됩니다. 일부 예는 과산화나드 나트륨 (Na 2 입니다 o 2 ), 과산화 칼륨 (k <서브> 2 o 2 ), 과산화물 마그네슘 (MGO) 등 공유 퍼 옥사이드 화합물은 분자 내 다른 원자에 직접 결합 된 O-O 단일 결합으로 구성되어; 예를 들어, 과산화수소 (H <서브> 2 o 2 ) 및 퍼 옥시 모노 술로 산 (H 2 그래서
퍼 옥사이드는 생물학적 시스템과 본질적으로 찾을 수 있습니다. 예를 들어, 우리 세포의 일부 효소는 과산화물을 사용하여 특정 반응을 촉매합니다. 일부 식물 종은 과산화물 화합물을 신호 화학 물질로 사용합니다. 과산화물은 실험실 규모 응용에도 사용됩니다. 유기 반응으로부터 항 마르 코프 니코프 생성물을 얻기 위해 유기 화학에서 매우 유용합니다.
과산화수소 수소
과산화수소는 분자식 H 2 를 갖는 과산화물 화합물입니다. o 2 . 4 개의 원자 사이의 모든 결합은 공유 결합이기 때문에 공유 화합물입니다. 두 산소 원자는 서로 결합됩니다. 2 개의 수소 원자는 산소 원자에 결합되어 산소 원자 당 하나의 수소 원자가. 과산화수소의 몰 질량은 약 34.014 g/mol입니다.
과산화수소는 물과 약간 다른 점도가있는 옅은 푸른 색의 액체입니다. 그것은 약산으로 간주됩니다. 산화 특성이 강하기 때문에 과산화수소는 표백 화합물의 산화제로 사용됩니다. 과산화수소는 불안정합니다. 산소 가스와 물로 빠르게 분해됩니다.
수 분자와 과산화수소 분자의 차이는 과산화수소 분자식에 존재하는 여분의 산소 원자 일 뿐이지 만 분자 구조는 서로 크게 다릅니다.
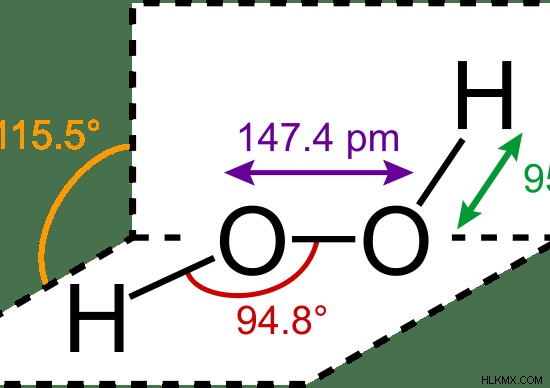
그림 2 :과산화수소의 화학적 특성
과산화수소는 의료 응용 분야뿐만 아니라 산업 응용 분야에서도 사용됩니다. 업계에서 과산화수소는 표백제의 표백 성분으로 사용됩니다. 의료 응용 분야에서는 소독제로 사용됩니다. 그 외에도 추진제로도 사용할 수 있습니다.
과산화수소와 과산화수소의 유사성
- 두 화합물 모두 산소 산소 단일 결합으로 구성됩니다.
- 둘 다 좋은 산화제입니다.
과산화수소와 과산화수소의 차이
정의
퍼 옥사이드 : 과산화물은 산소 산소 단일 결합으로 구성된 화합물입니다.
과산화수소 : 과산화수소는 분자식 H 2 를 갖는 과산화물 화합물입니다. o 2 .
자연
퍼 옥사이드 : 과산화물은 이온 성 화합물 또는 공유 화합물 일 수있다.
과산화수소 : 과산화수소는 공유 화합물입니다.
몰 질량
퍼 옥사이드 : 퍼 옥사이드의 몰 질량은 O-O 결합에 연결된 원자 또는 원자 그룹에 의존합니다.
과산화수소 : 과산화수소의 몰 질량은 약 34.014 g/mol입니다.
수소 원자의 존재
퍼 옥사이드 : 퍼 옥사이드는 O-O 단일 결합에 직접 결합 된 수소 원자로 구성 될 수 있거나 그렇지 않을 수 있습니다.
과산화수소 : 과산화수소는 본질적으로 O-O 단일 결합에 결합되는 2 개의 수소 원자로 구성됩니다.
결론
퍼 옥사이드는 산소-산소 단일 공유 결합으로 구성된 화합물입니다. 과산화수소는 또한 과산화물 화합물의 한 유형이다. 과산화물 화합물은 주로 이온 성 화합물 및 공유 화합물로서 2 개의 그룹으로 나눌 수있다. 그러나 과산화수소는 공유 화합물입니다. 이것이 과산화수소와 과산화수소의 주요 차이점입니다.