주요 차이 - 알칼리 대 알칼리성
알칼리 및 알칼리성 지구 금속은 기본 요소이며, 그들이 형성된 화합물은 또한 기본 화합물이기도합니다. 물에 첨가 될 때, 용액은 pH 7보다 높은 pH 값을 나타낸다. 이들 화합물은 매체의 산도를 중화 시키거나 감소시키는 것과 같은 다른 목적으로 사용된다. 알칼리 금속은주기 테이블의 그룹 1 금속 인 반면 알칼리 지구 금속은 그룹 2에 있습니다. 알칼리와 알칼리의 주요 차이점은 알칼리 금속의 주요 차이점은 하나의 원자가 전자를 가지고 있다는 것입니다.
주요 영역을 다루었습니다
1. 알칼리
- 정의, 속성, 예
2. 알칼리성이란?
- 정의, 속성, 예
3. 알칼리와 알칼리성의 유사점은 무엇입니까
- 일반적인 기능의 개요
4. 알칼리와 알칼리성의 차이점은 무엇입니까
- 주요 차이점 비교
주요 용어 :알칼리, 알칼리 금속, 알칼리성, 알칼리성 지구 금속, 주기율표, pH, 원자가 전자
alkali
알칼리라는 용어는 주기율표의 그룹 1 요소 (리튬, 나트륨, 칼륨 등)의 이름을 지정하는 데 사용됩니다. 이 요소는 알칼리 금속으로 알려져 있습니다. 이들 요소로부터 형성된 기본 화합물은 알칼리 화합물이다. 알칼리 화합물은 물에 첨가 될 때 OH 이온을 형성 할 수있는 물질이다. 따라서, 알칼리 화합물은 물에 용해되어 pH 7보다 높은 값을 갖는 용액을 제공한다. 모든 알칼리는 7보다 큰 pH 값을 갖는다. 이들은 기본 화합물이다.
.알칼리 물질은 빨간 리트머스의 색상을 파란색으로 바꿀 수 있습니다. 또한 최종 제품으로 소금과 물을 제공하는 산성 화합물과 반응 할 수 있습니다. 따라서, 알칼리 물질은 산성 용액을 중화시키는 데 사용될 수있다. 알칼리 금속은 매우 부드럽습니다 (칼을 사용하여 나트륨을 쉽게자를 수 있음). 이 요소들은 가장 바깥 쪽 궤도에 하나의 원자가 전자를 갖는다. 따라서, 그것들은 매우 반응성이 높은 요소입니다. 원자가 전자를 제거하여 +1 양이온을 형성 할 수 있습니다.
집중된 알칼리 형태에서는 부식성이며 피부 자극을 유발할 수 있습니다. 가장 일반적인 알칼리성에는 수산화물 및 탄산염이 포함됩니다. 산과 수산화물 사이의 반응은 소금과 물을 줄 것입니다. 산과 탄산염 사이의 반응은 염, 물 및 이산화탄소 가스를 제공합니다.

그림 1 :수산화 나트륨
예제
- 수산화 나트륨 (NAOH)
- 수산화 칼륨 (KOH)
- 산화 리튬 (li 2 o)
- 암모니아 (nh 3 )
alkaline
알칼리성이라는 용어는 주기율표의 그룹 2 요소 (마그네슘, 칼슘, 스트론튬 등)를 지명하는 데 사용됩니다. 이들은 알칼리성 지구 금속으로 알려져 있습니다. 이 화합물은 또한 물에 첨가 될 때 OH 이온을 형성한다. 알칼리성 화합물의 용액은 더 높은 pH 값을 갖는다 (> 7).
이 알칼리성 화합물은 또한 붉은 색 리트머스를 파란색으로 바꿀 수 있습니다. 그들은 기본 속성을 가지고 있습니다. 알칼리성 지구 금속은 알칼리 금속보다 단단합니다. 이들 요소는 2 개의 원자가 전자를 갖고 전자를 제거하여 양이온을 형성 할 수 있기 때문에 +2 양이온을 형성한다. 그러나, 이들 전자는 전자 쌍으로서 궤도에 있기 때문에, 이들 요소는 그다지 반응하지 않습니다.
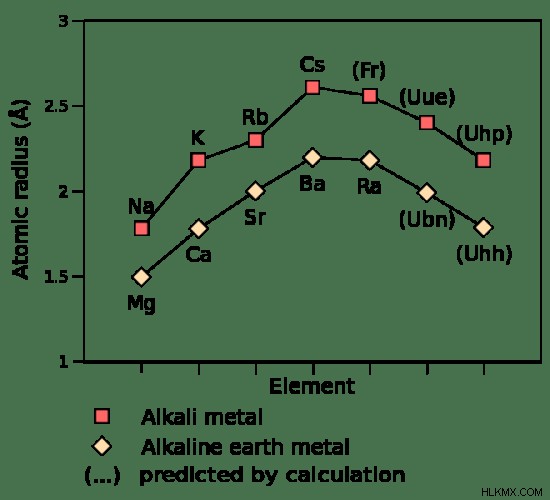
그림 2 :알칼리와 알칼리성 지구 금속의 원자 반경 비교
알칼리성 지구 금속은 알칼리 금속보다 원자 반경이 낮습니다. 이것은 전자와 양성자의 수가 인접한 그룹 1 요소보다 높기 때문입니다.
알칼리와 알칼리성의 유사성
- 둘 다 기본 특성을 가지고 있습니다.
- 둘 다 빨간색 리트머스를 파란색으로 바꿀 수 있습니다.
- 두 가지 유형의 화합물은> 7ph를 갖는 수용액을 형성 할 수 있습니다.
- 둘 다 물에 첨가 될 때 OH 이온을 형성 할 수 있습니다.
알칼리와 알칼리성의 차이
정의
알칼리 :Alkali라는 용어는주기 테이블의 그룹 1 요소를 지명하는 데 사용됩니다.
알칼리성 : 알칼리성이라는 용어는 주기율표의 그룹 2 요소를 지명하는 데 사용됩니다.
물리적 특성
알칼리 :알칼리 금속은 부드럽습니다.
알칼리성 : 알칼리성 지구 금속은 단단합니다.
원자가 전자
알칼리 :알칼리 요소에는 하나의 원자가 전자가 있습니다.
알칼리성 : 알칼리성 지구 금속에는 두 개의 원자가 전자가 있습니다.
양이온
알칼리 :알칼리 금속 형태 +1cations.
알칼리성 : 알칼리성 지구 금속은 +2 양이온을 형성합니다.
이온화 에너지
알칼리 :알칼리 금속은 이온화 에너지가 낮습니다.
알칼리성 : 알칼리성 지구 금속은 이온화 에너지가 더 높습니다.
결론
알칼리 금속은 주기율표의 그룹 1의 요소입니다. 알칼리성 지구 금속은 그룹 2의 요소입니다. 둘 다 기본 특성이 있습니다. 물에 첨가 될 때, 둘 다 pH 값이 더 높은 용액을 형성 할 수있다 (> pH). 알칼리와 알칼리성의 주요 차이점은 알칼리 금속은 하나의 원자가 전자를 갖는 반면 알칼리성 지구 금속은 2 개의 원자가 전자를 갖는 것입니다.