주요 차이 - 방향족 대 항리아 성 대 비 방향족
방향족은 PI 궤도에서 전자의 전자가 비편화하는 능력으로 인해 분자의 안정화가 향상되는 공액 사이클로 알켄의 특성입니다. 방향족 화합물은 비편 화 된 PI 전자를 갖는 고리 구조에 배열 된 탄소 및 수소 원자로 구성된 유기 화합물이다. 항아로 미티는 4N 전자 (N =0, 1, 2 등)를 갖는 PI 전자 시스템을 갖는 순환 분자의 존재이다. 항 아로마 성 화합물은 매우 불안정하므로 반응성이 있습니다. 비 방향족 화합물은 방향족이 아닌 분자입니다. 방향족 항아로 로틱과 비 방향족의 주요 차이점은 방향족은 (4N +2) 전자를 갖는 비편 재화 된 PI 전자 시스템을 의미하는 것을 의미하며, 항 아로마는 4 개의 전자를 갖는 비 국외 PI 전자 시스템을 갖는 반면 비 방향족은 해당 분자에 박 대신 전자 시스템이 없다는 것을 의미한다는 것입니다.
주요 영역을 다루었습니다
1. 향기로운
- 정의, 향기로운 요구 사항, Huckel 's Rule
2. antiaromatic
- 정의, antiaromatic 의 요구 사항
3. 비 방향족
- 정의, 비 방향 적이어야하는 요구 사항
4. 방향족 항아로틱과 비 방향족의 차이점은 무엇입니까
- 주요 차이점 비교
핵심 용어 :항아로 로틱, 방향족, 순환, 탈퇴, 허클 규칙, 비 방향족, PI 전자 시스템, 공명 효과

Aromatic
방향족 화합물은 반사 화 된 PI 전자를 갖는 고리 구조에 배열 된 탄소 및 수소 원자로 구성된 유기 화합물입니다. 방향족 탄화수소는 쾌적한 아로마로 인해 이름을 따서 명명되었습니다. 방향족 탄화수소는 본질적으로 주기적 구조입니다. 이것들은 또한 평면 구조입니다.
방향족 화합물은 공명 효과로 인해 매우 안정적입니다. 이는 방향족 화합물이 종종 단일 및 이중 결합을 함유하는 공명 구조로 표현되지만 실제 구조는 고리의 모든 원자 사이에 공유되는 비편성 전자를 갖는다. 탈소 화는 인접한 원자의 p 궤도의 겹치는 것을 말한다. 이 겹치는 것은 이중 결합이 활용된 경우에만 발생합니다. (컨쥬 게이션이 존재하면, 고리 구조의 모든 탄소 원자에는 p 궤도가 있습니다.)
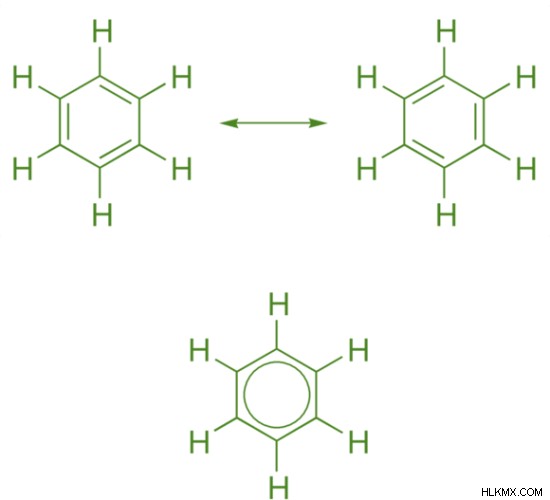
그림 1 :벤젠의 공명 구조
분자가 방향족 화합물로 지명 되려면 허클의 규칙 에 순종해야합니다. . 이 규칙은 다음과 같이 주어질 수 있습니다.
- 방향족 화합물은 4n + 2 pi 전자를 가져야합니다 (여기서 n은 정수 =0, 1, 2 등).
일반적으로 방향족 화합물은 비극성입니다. 그러므로 그들은 물에 비해 비밀다. 탄소 대 하수겐 비율은 방향족 화합물에서 적다. 대부분의 방향족 화합물은 전자 성 치환 반응을 겪습니다. 비편성 PI 전자의 존재로 인해, 방향족 고리에는 전자가 풍부하다. 따라서 Electrophiles는이 링을 공격하여 전자를 공유 할 수 있습니다.
방향족 화합물은 종종 석유 오일에서 얻습니다. 다수의 탄화수소 (PAH)는 환경 오염 물질 및 발암 물질로 간주됩니다.
antiaromatic
항아로 로이스 화합물은 순환, 평면 및 완전히 접합 된 분자이지만 4N Pi 전자로 구성된 분자입니다. 이들 항 아로마 성 화합물은 매우 불안정하여 반응성이다. 예를 들어, 사이클로 부타 디엔은 항 아로이 성입니다.
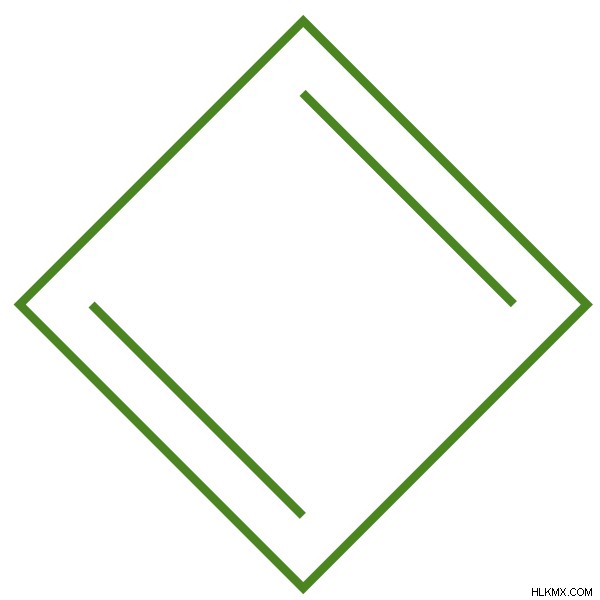
그림 2 :사이클로 부타디엔은 항아로 더 성 화합물 입니다
항 아로마 화합물은 허클의 규칙에 순종하지 않습니다. 그것들은 동일한 수의 PI 전자를 갖는 acyclic 화합물보다 항상 덜 안정적입니다. 그러나, 항아로 로이스 화합물은 공액 이중 결합의 존재로 인해 박전 된 PI 전자 시스템을 갖는다.
항아로 로이스 화합물은 순환 공액 PI 전자 시스템의 에너지를 측정함으로써 열역학적으로 인식 될 수 있습니다. 에너지는 항상 비교에 사용되는 기준 화합물보다 높을 것입니다.
비 방향족
비 방향족 화합물은 방향족이되기위한 요구 사항 중 하나 이상이 부족한 분자입니다. 평면 및 순환 구조, 완전히 접합 된 시스템입니다. 따라서 모든 지방족 화합물은 비 방향족입니다. 평면 인 일부 주기적 화합물조차도 공액 이중 결합의 부족으로 인해 비 방향족 일 수있다. 예를 들어, 1,3- 시클로 헥사 디엔은 평면적이고 순환이지만 이중 결합의 컨쥬 게이션이 없기 때문에 비 방향족 화합물입니다.
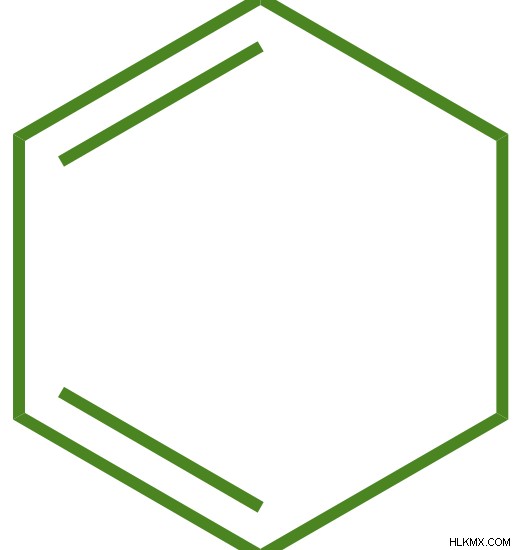
그림 3 :1,3- 사이클로 헥사 디엔은 비 방향족 화합물 입니다
방향족 항아로 로틱과 비 방향족의 차이
정의
방향족 : 방향족 화합물은 박대 된 PI 전자를 갖는 고리 구조에 배열 된 탄소 및 수소 원자로 구성된 유기 화합물이다.
antiaromatic : 항아로 로이스 화합물은 순환, 평면 및 완전히 접합 된 분자이지만 4N PI 전자로 구성된 분자입니다.
비 방향 : 비 방향족 화합물은 방향족에 대한 요구 사항 중 하나 이상이 부족한 분자입니다. 평면 및 순환 구조, 완전히 접합 된 시스템.
안정성
방향족 : 방향족 화합물은 안정적입니다.
antiaromatic : 항아로 로이스 화합물은 매우 불안정하다.
비 방향 : 비 방향족 화합물은 안정적입니다.
비편성
방향족 : 방향족 화합물에는 박전 된 PI 전자 시스템 및 4N + 2 PI 전자가 있습니다.
antiaromatic : 항아로 로이스 화합물은 박전 된 PI 전자 시스템 및 4N PI 전자를 갖는다.
비 방향 : 비 방향족 화합물은 박대 된 PI 전자 시스템을 사용하거나 없을 수 있습니다.
PI 전자
방향족 : 방향족 화합물은 4N + 2 PI 전자를 갖는다.
antiaromatic : 항아로 로이스 화합물은 4N Pi 전자를 갖는다.
비 방향 : PI 전자의 수는 비 방향족 화합물에 적용되지 않습니다.
반응성
방향족 : 방향족 화합물은 덜 반응성입니다.
antiaromatic : 항 아로마 성 화합물은 반응성이 높다.
비 방향 : 비 방향족 화합물은 덜 반응성입니다.
결론
방향족 항아로 로틱과 비 방향족의 주요 차이점은 방향족이 (4N +2) 전자를 갖는 비편정 된 PI 전자 시스템을 의미한다는 것을 의미하며, 4 개의 전자를 갖는 비서화 된 PI 전자 시스템을 갖는 반 인사 된 PI 전자 시스템을 갖는 반면 비 무자비 수단은 해당 분자에 비본화 된 전자 시스템이 없다는 것입니다.
.참조 :
1.“향기 성.” Chemistry LibreTexts, LibreTexts, 2016 년 9 월 18 일, 여기에서 사용할 수 있습니다.
2. Pooja Thakral. "방향족 방향성 비 방향족." LinkedIn SlideShare, 2016 년 12 월 4 일, 여기에서 구할 수 있습니다.
3. "반도성." Wikipedia, Wikimedia Foundation, 2017 년 11 월 23 일, 여기에서 구입할 수 있습니다.
이미지 제공 :
1. EDGAR181의“벤젠 공명 구조” - Commons Wikimedia
2를 통한 자신의 작업 (공개 도메인). Jake V - Commons Wikimedia
3을 통한 Jake V의 "Cyclobutadiene Structure2". Wickey-NL의“1,3- 시클로 헥사 디엔”-Commons Wikimedia를 통해 자신의 작업 (공개 도메인)