1. 반응물 :반응물은 반응에서 화학적 변화를 겪는 출발 물질 또는 물질이다. 그것들은 방정식의 왼쪽에 쓰여졌으며 플러스 (+) 표시로 분리됩니다.
2. 제품 :제품은 화학 반응의 결과로 형성된 물질입니다. 그것들은 방정식의 오른쪽에 기록되어 있으며 플러스 (+) 표시로 분리됩니다.
3. 계수 :계수는 반응에 관여하는 반응물 및 생성물의 상대적인 양을 나타내는 화학 공식 앞에 배치 된 수치 값이다. 계수는 방정식의 균형을 유지하여 각 요소의 원자 수가 양쪽에 보존되도록합니다.
4. 반응 화살표 :반응 화살표 (→)는 반응물을 생성물과 분리하고 화학적 변화의 방향을 나타냅니다. 반응물의 제품으로의 변환을 의미합니다.
5. 상태 기호 :첨자 또는 기호는 반응물 및 제품의 물리적 상태를 나타내는 데 사용될 수 있습니다. 공통 상태 기호에는 고체의 경우 (S), 액체의 경우 (L), 가스의 경우 (g), 수성 (물에 용해)이 포함됩니다.
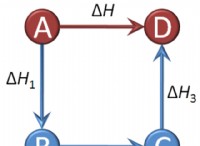
6. 열 또는 에너지 변화 :일부 화학 방정식에서, 반응 화살표 위 또는 아래에 열 또는 에너지 변화가 표시 될 수있다. 예를 들어, 상징 ΔH는 반응의 엔탈피 변화를 나타내며, 이는 발열 (열 방출)인지 흡열 (열을 흡수)인지를 나타냅니다.
7. 반응 조건 :온도, 압력 또는 촉매의 존재와 같은 특수 반응 조건은 필요한 경우 반응 화살표 위 또는 아래에 포함될 수 있습니다.
화학 방정식을 분석하고 해석함으로써, 반응의 화학량 론적 (정량적 관계)을 이해하고 반응물 및 생성물을 식별하며 반응 동안 발생하는 화학적 변화에 대한 통찰력을 얻을 수 있습니다.