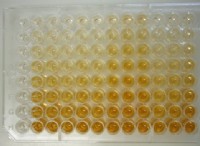
* 용해도 및 온도 : 액체에서 가스의 용해도는 액체 위의 가스의 부분 압력과 직접 관련이있다. 그러나 온도는이 관계에서 중요한 역할을합니다.
* 운동 에너지 : 온도를 늘리면 가스 분자의 운동 에너지가 증가합니다. 이 분자들은 더 빠르게 움직이고 더 많은 에너지를 가지므로 액체 상을 피하고 기체상으로 돌아갈 수 있습니다.
* 평형 이동 : 액체에 가스를 용해시키는 것은 평형 공정입니다. 온도를 증가 시키면 평형이 기체 상태로 이동하여 액체에 용해 된 가스의 양이 줄어 듭니다.
이런 식으로 생각하십시오 : 액체에 갇힌 가스를 상상해보십시오. 온도가 상승함에 따라 가스 분자는 흥분되고 더욱 격렬하게 "바운스"합니다. 그들은 액체에 그들을 잡고있는 세력에서 벗어나 위의 공기로 탈출 할 가능성이 더 높습니다.
예 :
* 탄산 음료 : 캔이나 소다 병을 열면 압력이 풀리고 음료의 온도가 증가하기 때문에 가스 (CO2)가 탈출합니다.
* 끓는 물 : 물이 끓으면서 산소 및 질소와 같은 용해 된 가스가 방출되어 기포가 형성됩니다.
예외 :
일반적인 규칙은 온도가 증가하면 가스 용해도가 감소하지만 몇 가지 예외가 있습니다. 암모니아 (NH3)와 같은 일부 가스는 실제로 더 높은 온도에서 물에 더 용해됩니다. 이러한 예외는 종종 가스와 용매 사이의 복잡한 화학적 상호 작용 때문입니다.
요약 : 가스 분자의 증가 된 운동 에너지가 용액으로부터의 탈출을 촉진하기 때문에 온도가 증가하면 가스가 액체에 용해되기가 더 어려워집니다.