다음은 고장입니다.
용해도에 영향을 미치는 요인 :
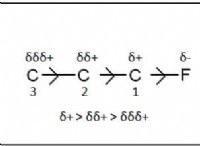
* 극성 : 물은 극지방 용매입니다. 극성 기능 그룹 (알코올, 카르 복실 산, 아민)을 갖는 유기 화합물은 물 분자와 수소 결합을 형성 할 수 있기 때문에 물에 용해 될 가능성이 높습니다.
* 크기와 모양 : 더 작고 컴팩트 한 유기 분자는 더 크고 더 복잡한 분자보다 물에 용해 될 가능성이 높습니다.
* 기능 그룹 : 기능 그룹의 존재와 본질은 용해도에 크게 영향을 미칩니다. 하이드 록실 (-OH), 카르 복실 (-COOH) 및 아미노 (-NH2)와 같은 극 기능 그룹은 수용성을 향상시킨다.
* 분자간 힘 : 반 데르 발스 힘 또는 수소 결합과 같은 유기 분자 내의 강한 분자간 힘은 물의 용해도를 방해 할 수 있습니다.
예 :
* 에탄올 (C2H5OH)은 물에 용해된다 물 분자와 수소 결합을 형성 할 수있는 극성 하이드 록실 그룹 (-OH)이 있기 때문입니다.
* 헥산 (C6H14)은 물에 불용성입니다 극성 기능 그룹이없는 비극성 탄화수소이기 때문입니다.
* 아세트산 (CH3COOH)은 물에 용해됩니다 극성 카르 복실 그룹 (-COOH)으로 인해.
* 벤젠 (C6H6)은 물에 불용성입니다 비극성 방향족 탄화수소이기 때문입니다.
일반적으로 :
* 비극성 유기 화합물은 일반적으로 물에 덜 용해됩니다.
* 극성 유기 화합물은 일반적으로 물에 더 용해됩니다.
주목하는 것이 중요합니다 :
* 용해도는 이진 개념이 아닌 스펙트럼입니다. 일부 유기 화합물은 부분적으로 물에 용해 될 수 있습니다.
* 온도 및 압력과 같은 다른 요인들도 용해도에 영향을 미칩니다.
따라서 모든 유기 화합물이 물에 덜 용해된다고 말하는 것은 부정확합니다. 물에서 유기 화합물의 용해도는 그들의 화학적 구조와 극 기능 그룹의 존재에 의존한다고 말하는 것이 더 정확하다. .