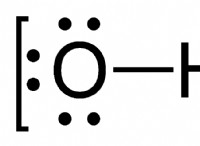이유는 다음과 같습니다.
* 가장 바깥 쪽 전자 : 알칼리 금속은 가장 외부 에너지 수준 (S- 궤도)에 단일 전자를 가지고 있습니다. 이 전자는 원자에 느슨하게 결합되어 쉽게 제거 할 수 있습니다.
* 반응성 : 이 단일 전자는 화학 반응에 참여하기를 간절히 원합니다. 알칼리 금속은 가장 바깥 쪽 쉘에서 안정적인 옥트 (8 전자)를 달성하기 위해이 전자를 쉽게 잃어 버리기 때문에 반응성이 높습니다. 전자의 이러한 손실은 양으로 하전 된 이온 (양이온)을 형성한다.
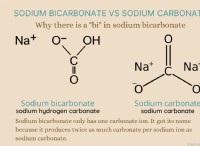
* 예 : 나트륨 (NA)은 가장 바깥 쪽 쉘 (3S¹)에 하나의 전자를 갖는다. 그것은이 전자를 쉽게 잃어 나온 이온을 형성합니다.
중요한 참고 : 알칼리 금속은 너무 반응하여 자연에서 순수한 형태로 발견되지 않습니다. 그들은 항상 화합물로 발견됩니다.