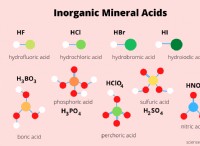
1. 황산염 이온 (so ²⁻)
* 이것은 부정적인 하전 된 이온이며 제조되지 않았습니다.
* 많은 미네랄, 특히 gypsum (caso₄ · 2h₂o) 에서 자연적으로 발견됩니다. 및 anhydrite (caso₄) .
* 또한 황산 (h₂so₄)의 주요 성분입니다. .
2. 황산염 염
* 이들은 황산염 이온이 다른 양성 이온 (양이온)과 결합 될 때 형성된 화합물입니다.
* 예에는 다음이 포함됩니다.
* 황산나트륨 (Na₂So₄)
* 황산 마그네슘 (MGSOA)
* 황산 암모늄 ((NHAT) ₂SOA)
* 황산염 염은 특정 염에 따라 다양한 방식으로 제조 될 수 있습니다.
* 자연 공급원 : 일부 황산염 염은 석고 또는 무수물과 같은 미네랄의 침착 물에서 직접 채굴됩니다.
* 황산을 다른 물질과 반응함으로써 : 예를 들어, 황산 나트륨을 염화나트륨 (SALT)과 반응시켜 황산나트륨을 생산할 수 있습니다.
* 산업 공정 : 일부 황산염 염은 인산의 생산과 같은 다른 산업 공정의 부산물입니다.
유황은 어디에서 왔습니까?
* 황산과 황산염을 만드는 데 사용되는 황은 다양한 공급원에서 비롯됩니다.
* 원소 황색 : 지하 예금에서 채굴.
* 황화수소 (H₂S) : 천연 가스 성분은 종종 황을 생산하기 위해 추출되고 가공됩니다.
* 황화물 미네랄 : 황철석과 같은 광석 (FES₂)은 황을 추출하기 위해 처리됩니다.
황산 제조 :
* 가장 일반적인 방법은 접촉 과정입니다 :
1. 황은 공기 중에 연소되어 이산화황을 생성합니다 (SO₂).
2. 이산화황은 촉매를 사용하여 트라이 산화 황 (SO₃)으로 산화된다.
3. 황산을 물에 용해시켜 황산을 생산합니다 (H₂SOA).
황산염 염은 황산을 다른 물질과 반응하여 제조 할 수 있습니다.
요약하면, 황산염 이온은 자연적으로 발생하고 황산염 염은 다른 공급원의 황을 사용하여 다양한 방식으로 제조 될 수 있습니다. 가장 일반적인 방법은 황산 생산을위한 접촉 공정과 관련이 있습니다.