기본 빌딩 블록 :
* 매우 작습니다 : 원자는 해당 요소의 화학적 특성을 유지하는 요소의 가장 작은 단위입니다. 그것들은 엄청나게 작으며 나노 미터 (1 나노 미터 =10 억 미터)의 순서를 측정합니다.
* 아 원자 입자 : 원자는 세 가지 주요 아 원자 입자로 구성됩니다.
* 양성자 : 핵에 위치한 양으로 하전 된 입자.
* 중성자 : 핵에 위치한 중립적으로 하전 된 입자.
* 전자 : 전자 쉘이라는 특정 에너지 수준에서 핵을 공전하는 음으로 하전 된 입자.
* 중립 전하 : 원자는 일반적으로 같은 수의 양성자와 전자를 가지므로 전반적인 전하를 제공합니다.
속성 정의 :
* 원자 번호 : 원자의 핵에서 양성자의 수. 이 숫자는 요소를 고유하게 식별합니다. 예를 들어, 모든 탄소 원자에는 6 개의 양성자가 있습니다.
* 원자 질량 : 원자의 핵에서 총 양성자 및 중성자 수. 일반적으로 원자 질량 단위 (AMU)로 표현됩니다.
* 동위 원소 : 동일한 요소의 원자는 다른 수의 중성자를 가질 수 있으며, 원자 질량이 다를 수 있습니다. 이것을 동위 원소라고합니다. 예를 들어, 탄소 -12 및 탄소 -14는 탄소의 동위 원소이다.
* 전자 구성 : 원자의 전자 쉘에서 전자의 배열은 화학적 거동을 결정합니다. 원자가 쉘이라고하는 가장 바깥 쪽 쉘이 특히 중요합니다.
* 전기 음성 : 화학적 결합으로 전자를 유치하는 원자의 능력 측정.
화학 행동 :
* 본딩 : 원자는 서로 상호 작용하여 화학적 결합을 형성 할 수 있습니다. 다음을 포함하여 여러 유형의 채권이 있습니다.
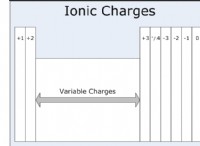
* 이온 결합 : 원자 사이의 전자의 전달, 이온 (하전 된 원자)의 형성을 초래한다.
* 공유 결합 : 원자 사이의 전자 공유.
* 반응성 : 원자가 화학 반응에 참여하는 경향. 부분적으로 채워진 원자가 껍질을 갖는 원자는 일반적으로 더 반응성입니다.
기본을 넘어서 :
* 양자 역학 : 원자에서 전자의 거동은 입자의 파도와 같은 특성을 설명하는 양자 역학에 의해 지배된다.
* 분광학 : 원자 흡수 분광법 및 방출 분광법과 같은 기술은 방출 또는 흡수하는 빛을 검사함으로써 물질의 구성을 분석하는 데 사용될 수 있습니다.
이 점들에 대해 자세히 설명하려면 알려주세요!