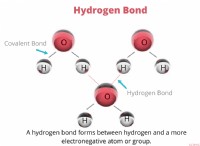
* 화학 결합 : 물 분자는 수소와 산소 원자 사이의 강한 공유 결합에 의해 함께 유지된다. 소금은 물에 용해되어 이온 (Na⁺ 및 Cl⁻)을 형성하지만, 이들 이온은 물 분자 내의 공유 결합과 상호 작용하지 않는다.
* 전기 분해 : 수소를 물과 분리하려면 전기 분해라는 과정을 사용해야합니다. 여기에는 물을 통해 전류를 통과시키는 것이 포함되며, 이는 물 분자를 수소 가스 (HAT)와 산소 가스 (O₂)로 분해합니다.
소금이 물에 녹을 때 발생하는 일에 대한 고장이 있습니다.
1. 용해 : 염 결정은 개별 이온으로 분리됩니다 (Na⁺ 및 Cl⁻).
2. 수화 : 이들 이온은 물 분자로 둘러싸여 수화 된 이온을 형성한다. 물 분자는 하전 된 이온에 끌립니다.
3. 솔루션 : 소금 이온은 이제 물 전체에 분산되어 염 용액을 형성합니다.
중요한 참고 : 소금은 수소를 물에서 분리하지 않지만 물의 전기 전도성에 영향을 줄 수 있습니다. 그렇기 때문에 짠 물이 순수한 물보다 더 나은 전기 도체 인 이유이므로 바닷물 근처에 전기 가전 제품을 사용하는 것이 위험합니다.