1. 본드 강도 :
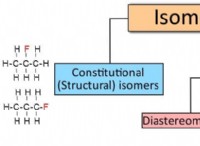
* 탄소-수소 (C-H) 및 탄소 염소 (C-Cl) 결합 : 이러한 결합은 실리콘 상대 (SI-H 및 SI-CL)보다 상당히 강합니다. 이는 실리콘에 비해 탄소 원자의 크기가 작기 때문에 궤도 겹치고 공유 결합이 더 강해집니다.
* 실리콘-하이드로겐 (SI-H) 및 실리콘 클로린 (SI-CL) 결합 : 이러한 결합은 실리콘의 크기가 크고 효과적인 궤도 겹침으로 인해 약합니다. 이것은 물 분자에 의한 공격에 더 취약하게 만듭니다.
2. 극성과 반응성 :
* 탄소 : C-H 및 C-Cl 결합은 비교적 비극성이므로 극성 물 분자에 대해 덜 반응성이 있습니다.
* 실리콘 : SI-H 및 SI-CL 결합은 실리콘과 다른 요소 사이의 전기 음성 차이로 인해 더 극성입니다. 이 극성은 물에 의한 친 핵성 공격에 더 취약하게 만듭니다.
3. 입체 효과 :
* 탄소 : 더 작은 크기의 탄소 원자는 입체 방해가 적어 물 분자가 C-H 및 C-Cl 결합에 접근하고 공격하기가 더 어려워집니다.
* 실리콘 : 더 큰 크기의 실리콘 원자는 더 많은 입체 장애를 생성하여 물 분자가 Si-H 및 SI-CL 결합에 더 쉽게 접근 할 수있게한다.
가수 분해 반응 :
가수 분해 반응은 물 분자를 첨가함으로써 결합의 파괴를 포함한다. 예를 들어, 실리콘 화합물의 경우 :
* si-cl + h2o-> si-oh + hcl
약화 된 SI-CL 결합은 물에 의한 공격에 더 취약하여 SI-OH (Silanol) 그룹 및 HCl의 형성으로 이어진다.
요약 :
CH4 및 CCL4와 같은 탄소 화합물에서 더 강한 결합, 낮은 극성 및 덜 입체 장애의 조합은 실리콘 유사체에 비해 가수 분해에 더욱 저항력이있다.