이유는 다음과 같습니다.
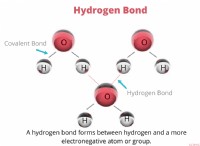
* CO2 및 탄산 산 : CO2가 물에 용해되면 탄산산 (H2CO3)을 형성합니다. 탄산은 약산으로 물의 이온으로 완전히 분리되지 않음을 의미합니다. 그러나 그것은 빗물의 산도에 기여합니다.
* 비의 자연 pH : 순수한 물의 pH는 7이며, 이는 중성입니다. 그러나 빗물의 천연 pH는 일반적으로 약 5.6이므로 약간 산성이됩니다. 이것은 용해 된 CO2로 형성된 탄산 때문입니다.
자연 산도를 구별하는 것이 중요합니다 및 산성 비 . 산성 비는 5.6보다 낮은 비를 의미하며, 주로 화석 연료 연소와 같은 인간 활동으로 인해 이산화황 (SO2)과 질소 (NOX)가 대기로 방출됩니다. 이 오염 물질은 물과 반응하여 황산 (H2SO4)과 질산 (HNO3)을 형성하여 비가 훨씬 더 산성으로 만듭니다.
따라서 비는 용해 된 CO2로 인해 자연적으로 약간 산성이지만 "산성 비"라는 용어는 인간이 부여 된 오염으로 인해 훨씬 더 산성 인 비를 의미합니다.