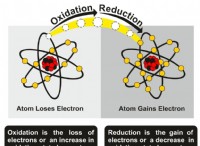
이유는 다음과 같습니다.
* 이온화 에너지 : 리튬은 나트륨보다 이온화 에너지가 더 높다. 이것은 나트륨 원자보다 리튬 원자에서 전자를 제거하기 위해 더 많은 에너지가 필요하다는 것을 의미합니다. 이로 인해 리튬이 전자를 잃고 화학 반응에 참여할 가능성이 높아집니다.
* 전기 양성 : 리튬은 나트륨보다 전기 양성이므로 전자를 잃고 양성 이온을 형성하는 경향이 더 강합니다.
* 원자 크기 : 리튬은 나트륨보다 작습니다. 이 작은 크기는 가장 바깥 쪽 전자가 핵에 의해 더 단단히 고정되어있어 유효 핵 전하가 더 높아집니다. 이로 인해 리튬이 전자를 잃고 반응에 더 쉽게 참여할 수 있습니다.
요약 : 더 높은 이온화 에너지, 더 큰 전기 양성 및 작은 원자 크기의 조합은 리튬이 나트륨보다 더 반응성이 높은 요소를 만듭니다.