* pH 및 산도 : pH가 낮을수록 더 산성 용액을 나타냅니다.
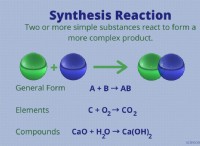
* 이산화탄소 및 탄산 산 : 이산화탄소가 혈액에 용해되면 물과 반응하여 탄산을 형성합니다 (H2CO3). 이 반응은 탄수화물 무수 효소라고 불리는 효소에 의해 촉매된다.
* 탄산산 해리 : 탄산은 수소 이온 (H+) 및 중탄산염 이온 (HCO3-)으로 분리 될 수있는 약산이다.
* 수소 이온 및 pH : 수소 이온 (H+)의 혈액 내 방출은 pH를 낮추어 더 산성으로 만듭니다.
pH 조절의 중요성 :
안정적인 혈액 pH를 유지하는 것은 정상적인 신체 기능에 중요합니다. 신체에는 다음을 포함하여 pH를 조절하는 메커니즘이 있습니다.
* 호흡 : 호흡 증가 (과 호흡)는 혈액에서 CO2를 제거하여 pH를 증가시키는 데 도움이됩니다.
* 신장 : 신장은 과도한 수소 이온을 걸러내어 pH 균형을 유지하는 데 도움이됩니다.
중요한 참고 : 이산화탄소는 혈액 pH를 낮추는 반면, 신체의 pH 조절 시스템은 좁은 범위 내에서 균형 잡힌 pH를 유지하기 위해 끊임없이 작용합니다.