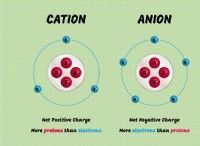
* 용액에서의 부분 이온화 : 약산은 용액에서 부분적으로 이온화 (해리)만이 이온 (H+ 및 컨쥬 게이트 염기)으로 완전히 분리되지 않는다는 것을 의미합니다. 이것은 거의 완전히 이온화하는 강산과 대조적입니다.
* KA 값이 낮습니다 : 산 분리 상수 (KA)는 산의 강도를 측정 한 것입니다. 약산은 강산에 비해 더 작은 KA 값을 갖는다.
* 동일한 농도에서 강산보다 높은 pH : 이들이 이온화되기 때문에, 약산은 용액에서 H+ 이온이 적어 더 높은 pH (산성이 적음)를 생성한다.
* 버퍼 역할을 할 수 있습니다. 약산은 그들의 컨쥬 게이트 염기와 함께 pH의 변화에 저항하는 완충액을 형성 할 수있다.
* 예 : 아세트산 (CH3COOH), 탄산산 (H2CO3) 및 구연산은 약산의 일반적인 예입니다.
이러한 특성에 대한 자세한 내용을 원하시면 알려주세요!