반응 유형 :
* 발열 : 음의 델타 H 값 (-74.9 kJ/mol)은 반응이 주변의 열을 방출 함을 나타냅니다. 이것은 발열 반응으로 만듭니다.
열역학적 고려 사항 :
* 호의 : 부정적인 엔탈피 변화는 반응이 열역학적으로 유리하다는 것을 의미합니다. 즉, 표준 조건에서 자발적으로 진행됩니다.
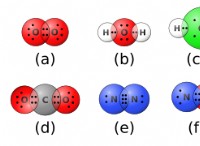
화학 방정식 :
* 균형 : 방정식 C + 2H2-> CH4는 균형을 이루어 반응의 양쪽에있는 각 원소의 원자 수가 동일합니다.
전체 프로파일 :
반응 C + 2H2-> CH4는 매우 유리한 발열 반응 입니다. 그것은 메탄 가스를 생성합니다. 이 반응은 천연 가스 산업에서 중요하며 유기 화학의 근본적인 반응입니다.
추가 메모 :
*이 반응은 합리적인 속도로 진행하기 위해서는 일반적으로 니켈 (일반적으로 니켈)이 필요합니다.
* 반응은 고온과 압력 하에서 반전 될 수 있지만 일반적으로 많은 에너지 입력이 필요하기 때문에 반대로 사용되지 않습니다.
이 반응에 대해 다른 질문이 있으면 알려주세요!