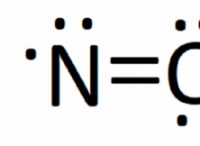* 화합물 둘 이상의 다른 요소가 고정 비율로 화학적으로 결합 될 때 형성됩니다.
* 요소 더 간단한 물질로 분해 될 수없는 순수한 물질입니다.
예를 살펴 보겠습니다.
* 물 (h>o) : 수소 (H)와 산소 (O)의 두 가지 요소로 구성됩니다. 이들은 2 :1 비 (모든 산소 원자에 대해 2 개의 수소 원자)로 화학적으로 결합됩니다. 이것은 물을 화합물로 만듭니다 .
* 산소 가스 (O₂) : 하나의 요소로만 구성됩니다 :산소 (O). "2"첨자는 2 개의 산소 원자가 함께 결합되어 있음을 나타냅니다. 그러나 여전히 요소로 간주됩니다 하나의 유형의 원자로 만 구성되어 있기 때문입니다.
주요 차이 : 정의 요인은 다른 의 존재입니다 화합물의 요소. 산소 가스는 함께 결합되어 있어도 산소 원자 만 포함합니다.
이런 식으로 생각하십시오 :물을 수소와 산소로 분해 할 수 있지만 산소 가스를 더 간단하게 분해 할 수는 없습니다.