* 이온 성 화합물은 정전기 인력에 의해 형성된다 : 이온 결합은 양으로 하전 된 이온 (양이온)과 음이온 (음이온) 사이의 인력으로부터 발생한다.
* 중립 전하는 목표입니다. 안정적인 화합물이 존재하기 위해서는 양전자와 음전하가 서로를 취소해야합니다.
* 밸런싱 하위 스크립트는 중립을 달성합니다. 화학 공식에서 첨자를 조정함으로써 존재하는 각 이온의 수를 제어 할 수 있습니다. 이를 통해 총 양전하가 총 음전하와 같은 균형을 달성 할 수 있습니다.
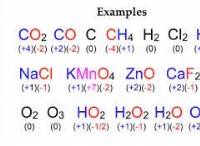
예 :
* 염화나트륨 (NaCl) : 나트륨 (NA)은 +1 전하를 갖고 염소 (CL)는 -1 전하를 갖는다. 하나의 나트륨 이온은 하나의 클로라이드 이온의 균형을 유지하여 중성 화합물을 초래합니다.
* 클로라이드 마그네슘 (mgcl₂) : 마그네슘 (mg)은 +2 전하를 갖고 염소 (CL)는 -1 전하를 갖는다. 우리는 마그네슘의 +2 전하의 균형을 잡으려면 2 개의 클로라이드 이온이 필요하여 중성 화합물을 초래합니다.
균형을 맞추지 않은 결과 :
* 불안정한 화합물 : 불균형 화합물은 순 양성 또는 음전하를 가지므로 반응성이 높고 불안정합니다.
* 잘못된 공식 : 화학적 공식은 화합물의 실제 조성을 정확하게 나타내지 않을 것이다.
요약하면, 이온 성 화합물의 숫자 균형은 다음과 같습니다.
* 화합물이 전기적으로 중립적인지 확인하십시오.
* 이온들 사이의 매력적이고 반발력을 균형있게 조정하여 안정성을 달성하십시오.
* 화합물의 올바른 조성을 나타냅니다.