어금니 농도 이해 (Molarity)
* Molarity 용액에서 용질의 농도의 척도입니다. 용액 리터당 용질의 두부 수로 정의됩니다.
* 몰스 물질의 양에 대한 측정 단위입니다. 모든 물질의 한 몰에는 6.022 x 10^23 개의 입자 (Avogadro의 수)가 포함됩니다.
물의 몰 농도 계산
1. 물의 밀도 : 4 ° C에서의 순수한 물의 밀도는 1 g/ml입니다.
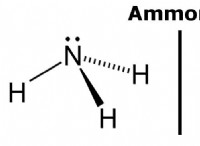
2. 물 질량 : 물 (H₂O)의 몰 질량은 18.015 g/mol (수소의 경우 2 x 1.008 g/mol + 15.999 g/mol)입니다.
3. 변환 : 이 값을 사용하여 어금니 농도를 계산할 수 있습니다.
* 1 g/ml * (1 ml/1 cm³) * (1000 cm³/1 l) =1000 g/L (이 밀도를 g/ml에서 g/l로 변환합니다)
* (1000 g/l)/(18.015 g/mol) =55.51 mol/l
따라서 물의 몰 농도는 약 55.56m입니다.
중요한 참고 : 이 계산은 우리가 4 ° C에서 순수한 물을 다루고 있다고 가정합니다. 따라서 밀도와 물의 몰 농도는 온도에 따라 약간 변할 수 있습니다.