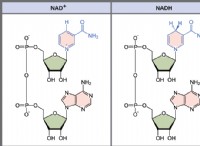
1. 산화 감소 (산화) 반응 :
* 산화 : 화학 종에 의한 전자 손실.
* 감소 : 화학 종에 의한 전자의 이득.
이러한 반응은 항상 동시에 발생합니다. 한 종은 전자를 잃고 (산화되어 있음), 다른 종은 전자를 얻습니다 (감소).
전기 화학에서 연구 된 산화 환원 반응의 예 :
* 물의 전기 분해 : 물은 전류를 통과시켜 수소와 산소 가스로 분해됩니다.
* 금속 부식 : 금속은 환경과 반응하여 전자를 잃고 산화물을 형성합니다.
* 배터리 : 배터리의 화학 반응은 전자의 전달을 통해 전류를 생성합니다.
* 연료 전지 : 화학 에너지는 연료를 산화제와 반응하여 전기 에너지로 변환됩니다.
2. 전극 반응 :
이들은 전극-전해질 인터페이스에서 발생하는 특정 유형의 산화 환원 반응입니다. . 그들은 전극 용액에서 전극과 화학 종 사이의 전자의 전달을 포함한다.
전극 반응의 유형 :
* 양극 반응 : 산화가 발생하는 양극에서 발생합니다.
* 음극 반응 : 감소가 발생하는 캐소드에서 발생합니다.
전극 반응의 예 :
* 전기 도금 : 용액의 금속 이온은 캐소드에서 감소되어 전극에 얇은 금속 층을 베스팅한다.
* 전기 화학 센서 : 분석 물 분자는 전극 표면에서 반응하여 측정 가능한 전기 신호를 생성합니다.
* 전기 화학 합성 : 전극 반응을 제어함으로써 새로운 화합물이 합성된다.
전반적으로 전기 화학은 다음과 같은 반응에 중점을 둡니다.
* 전자 전달은 중심 공정입니다.
* 전기의 흐름이 관련되어 있습니다.
* 전극은 반응을 촉진하는 데 중요한 역할을합니다.
이러한 반응을 연구함으로써 우리는 화학 공정에 대한 더 깊은 이해를 얻고 새로운 기술을 개발하며 다양한 응용 분야를위한 혁신적인 솔루션을 만듭니다.