* 혼성화 : sp³
* 기하학 : 사면체
* 결합 각도 : 109.5 °
* 시그마 채권 수 : 4
* 고독한 쌍의 수 : 0
설명 :
1. 혼성화 : 메탄의 탄소 원자에는 4 개의 원자가 전자가 있습니다. 4 개의 수소 원자와 4 개의 동등한 결합을 형성하기 위해, Sp³ 혼성화를 겪는다. 이것은 4 개의 Sp³ 궤도를 형성하기 위해 1 개의 2s 궤도 및 3 개의 2p 궤도의 탄소 하이브리드 화를 의미합니다. 이 sp³ 궤도는 사면형 모양으로 배향됩니다.
2. 기하학 : 4 개의 sp³ 궤도에서 전자 쌍 사이의 SP³ 혼성화 및 반발로 인해, 메탄의 탄소 원자는 사면체 형상을 채택한다. 이것은 4 개의 수소 원자가 정기 사면체의 모서리의 탄소 원자 주위에, 결합 각도는 109.5 ° 인 것을 의미합니다.
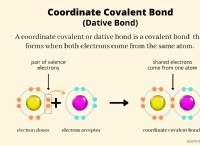
3. 본딩 : 탄소 원자의 4 개의 Sp³ 궤도 각각은 수소 원자의 1s 궤도와 시그마 결합을 형성한다. 이로 인해 4 개의 C-H 단일 결합이 발생합니다.
4. 고독한 쌍 : 탄소는 메탄에 고독한 쌍이 없습니다. 모든 원자가 전자는 결합에 관여합니다.
요약 : 메탄의 탄소 원자는 sp³ 하이브리드 화되고, 사면체 형상을 가지며, 수소 원자와 4 개의 시그마 결합을 형성한다. 고독한 쌍이 없습니다.