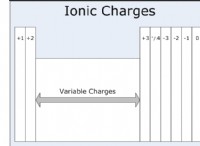
고장은 다음과 같습니다.
* 산 : 산은 물에 용해 될 때 수소 이온 (H+)을 기증하는 물질입니다. 예는 염산 (HCl), 황산 (H2SO4) 및 질산 (HNO3)을 포함한다.
* 금속 : 금속은 전자를 쉽게 잃어 양성 이온 (양이온)을 형성하는 요소입니다. 아연 (Zn), 마그네슘 (mg) 및 철 (Fe)이 그 예를 포함합니다.
반응 :
산이 금속과 반응 할 때, 산은 수소 이온 (H+)을 금속에 전달한다. 금속은 전자를 잃고 양으로 하전 된 이온을 형성합니다. 수소 이온은 전자를 얻고 수소 가스 (H2)를 형성하며, 이는 기포로 방출됩니다.
일반 방정식 :
산 + 금속 → 소금 + 수소 가스
예 :
염산 (HCL)은 아연 (Zn)과 반응합니다.
2 HCL + Zn → ZnCl2 + H2
* HCl : 염산
* Zn : 아연
* zncl2 : 염화 아연 (소금)
* H2 : 수소 가스
중요한 참고 :
모든 금속이 모든 산과 반응하는 것은 아닙니다. 산과의 금속의 반응성은 반응성 시리즈에서의 금속의 위치와 산의 강도와 같은 인자에 의존한다.