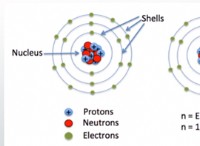
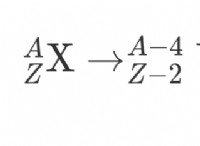* 마그네슘 이온의 가수 분해 : 마그네슘 이온 (mg²⁺)은 가수 분해를 겪습니다. 이는 물 분자와 반응합니다. 이 반응은 평형 반응입니다.
mg²⁺ (aq) + h₂o (l) ⇌ mgoh⁺ (aq) + h⁺ (aq)
* 평형의 이동 : 반응은 소량의 HAT 이온의 형성을 선호하며, 이는 용액의 약간 산성적인 특성에 기여한다. 이것은 mgoh the 이온이 약산이기 때문에 용액에서 완전히 이온화되지 않기 때문입니다.
* 전반적인 효과 : mg²⁺의 가수 분해는 h⁺ 이온의 농도가 약간 증가하여 용액을 약간 산성으로 만듭니다. 그러나 산도는 약하고 용액은 거의 중립으로 간주됩니다 .
중요한 참고 : 염화 마그네슘 용액의 pH는 그 농도에 의존 할 것이다. 더 농축 된 용액은 희석 용액보다 pH (산성)가 약간 낮습니다.